Фармакологическая помощь спортсмену: коррекция факторов, лимитирующих спортивный результат
О. С. Кулиненков
Оглавление
Предисловие
1. Факторы, ограничивающие работоспособность спортсмена
2. Систем клеточной регуляции на молкулярном уровне
3. Коррекция факторов, ограничивающих работоспособность спортсмена
4. Свободнорадикальные процессы при больших физических нагрузках
5. Микроциркуляция, реология, свертываемость крови
6. Иммунный статус спортсмена
7. Эндокринная система
8. Центральная нервная система, периферическая нервная система, вегетативная нервная система
9. Сократительная способность миокарда
10. Функции печени
11. Функции почек
12.Эндогенная интоксикация
13. Профилактика дисбактериоза
14. Восстановление мышц, связок, суставов при травме
15. Актуальные проблемы женского спорта
16. Десинхроноз (нарушение суточного динамического стереотипа)
Фармакологическая поддержка спортивных качеств
Вспомогательные средства восстановления
2. Клеточное дыхание работающих мышц
Гипоксия
Гипоксия тканей (кислородная недостаточность) –
широко распространенное явление, встречающееся в результате неблагоприятных
изменений в окружающей среде, при различных патологических состояниях, а также
при тренировочном процессе.
Причины появления гипоксии могут быть различными, но
ответная реакция организма носит неспецифический характер и в своем развитии
проходит несколько стандартных фаз. На каждой из них происходит последовательное
урезание энергетических возможностей. Поэтапное выключение фрагментов
дыхательной цепи по мере снижения содержания кислорода в тканях является
приспособительной реакцией организма на быстро ухудшающиеся условия среды.
Снижение энергопродуцирующих функций клеток до определенного предела имеет
обратимый характер, но при интенсивном развитии гипоксии или значительной ее
продолжительности изменения приобретают необратимый характер. Знание механизмов
повреждения тканей при гипоксии необходимо для наиболее эффективной коррекции
этого патологического состояния.
Митохондрии – субклеточные элементы, в которых
совершаются основные энергопреобразующие процессы. В последние годы активно
разрабатывается новая область медицины – митохондри-альная. Установлено, что
более 100 заболеваний вызваны различными нарушениями функционирования
митохондрий.
Сегодня устройство митохондриальной дыхательной цепи и
механизм ее работы обсуждаются с единых позиций во всех авторитетных изданиях, а
четверть века назад на научных конференциях шли ожесточенные споры между
представителями различных школ биоэнергетиков.
Английским биохимиком Питером Митчеллом (Mitchell P., 1961)
предложена хемиосмотическая гипотеза.
Известно, что окисление дыхательных субстратов кислородом
катализируется дыхательными ферментами, расположенными во внутренней мембране
митохондрий. По данной гипотезе окисление субстрата ферментом – акцептором
электронов – происходит на одной из сторон мембраны. В результате этой реакции
электрон присоединяется к ферменту и образовавшийся протон высвобождается из
мембраны и уходит в воду. Затем электрон переносится ферментом на другую сторону
мембраны, и там он восстанавливает кислород или другой фермент, проявляющий
акцепторные свойства к электрону. При восстановлении кислорода или фермента
происходит связывание протонов по другую сторону мембраны.
По хемиосмотической гипотезе в процессе дыхания происходит
направленный перенос протонов из одного отсека в другой, а разделительная
мембрана препятствует восстановлению равновесия между отсеками. Концентрирование
протонов по одну сторону мембраны в процессе дыхания представляет собой
осмотическую работу по переносу ионов в пространстве против градиента их
концентрации. В процессе окисления субстрата и восстановления кислорода
совершается также химическая работа.
Главная отличительная особенность мембранных окислительных
процессов, подмеченная Митчеллом, заключается в одновременном выполнении двух
видов работ – химической и осмотической. Эта особенность и определила название
выдвинутой гипотезы.
По этой гипотезе образование АТФ в процессе окислительного
расщепления субстрата происходит следующим образом: осмотическая энергия,
накопленная в виде разности концентраций протонов между двумя отсеками,
разделенными мембраной, расходуется на химическую работу, т е. на синтез АТФ.
Гениальное изобретение природы – система митохондриального
окисления субстрата – выполняет не только осмотическую и химическую, но и
электрическую работу. Выбрасывая из одного резервуара однозарядные ионы и
перенося их через мембрану в другой резервуар, такая система осуществляет
зарядку биологической мембраны как электрического конденсатора, когда по разные
стороны мембраны концентрируются ионы с противоположными зарядами.
Получил неопровержимое подтверждение фундаментальный факт
(Скулачев В.П.), вытекающий из хемиосмотической гипотезы, что сопряжение
процессов дыхания и фосфорилирования возможно только при наличии целостной
мембраны, надежно разделяющей разнозарядные ионы в своих отсеках. При
повреждении мембран различными веществами (в том числе оксидантами) синтез АТФ
прекращается.
Основные
энергопреобразующие процессы совершаются в митохондриях. Поломка отдельных
элементов в этой структуре ведет к нарушению энергетического гомеостаза с
серьезными последствиями для клетки, органа или организма в целом. Группа
ферментов, локализованная по внутренней мембране митохондрий и участвующая в
процессах биотрансформации энергии, получила название дыхательной цепи.
Принято считать, что митохондриальная цепь состоит из
четырех групп ферментов и белков, компактно локализованных во внутренней
мембране митохондрий (Рубин А., Шинкарев В.П.). Подобные группы ферментов
принято называть комплексами. Перенос восстановительных эквивалентов от
комплекса к комплексу может быть реализован только с использованием
низкомолекулярных переносчиков, способных участвовать в
окислительно-восстановительных реакциях. Подобных переносчиков в организме
известно два: убихинон, цитохром С.
Убихинон обеспечивает связь между комплексом I и II,
цитохром С – между III и IV.
Важно отметить, что хотя оба переносчика выполняют сходные
функции в общей мембране митохондрии, их работа организована таким образом, что
они не мешают друг другу. Убихинон функционирует в толще мембраны, а цитохром С
мигрирует по наружной ее поверхности. Пространственное разделение обоих потоков
позволяет исключить случаи транспортного хаоса.
В качестве энергетического субстрата комплекс I использует
НАНД (никотинамидадениндинуклеотид), образующийся в процессах как аэробного, так
и анаэробного окисления субстратов. Комплекс II катализирует реакции окисления
сукцината, образующегося в цикле трикарбоновых кислот (цикл Кребса).
Кислород является субстратом митохондриальной дыхательной
цепи. Дефицит кислорода ведет к ограничению, а при полном прекращении его
поступления в организм к быстрой дезорганизации работы дыхательной цепи, ее
мультиферментной системы. Главным результатом в этом случае становится истощение
клеточных запасов макроэргов и повреждение энергопребразующих механизмов. Такую
гипоксию в настоящее время принято называть биоэнергетической. При нарушении
энергетических потоков наступает состояние гипоксии тканей.
В зависимости от причин, вызывающих энергетический дефицит,
различают четыре вида гипоксии. По сути, биоэнергетическая гипоксия –
обязательный этап в каждом из четырех типов.
Гипоксическая гипоксия возникает при снижении
парциального давления кислорода в легочных альвеолах, что чаще всего наблюдается
при расстройстве системы внешнего дыхания или при подъеме на высоту, в горах.
Гемическая гипоксия наступает при дефиците или
нарушении функционирования эритроцитарных клеток, специализирующихся на доставке
кислорода из легких в ткани-потребители. При этом различают анемический тип
гемической гипоксии, связанный с уменьшением концентрации гемоглобина, и
патологический тип, наблюдаемый при инактивации гемоглобина.
Если гипоксия тканей связана с нарушением кровообращения,
выделяют циркуляторную гипоксию. Она может быть связана как с местным,
так и системным нарушением кровообращения или с перфузией ткани кровью.
Отдельно рассматривают случаи тканевой гипоксии,
когда р02 в крови соответствует норме, гемоглобин эффективно связывает
молекулы кислорода, а кровь успешно доставляет его в ткани, но последние не в
состоянии его использовать. Тканевая гипоксия наступает при отравлении
митохондриальных ферментов дыхательными ядами, например цианидами или угарным
газом, при дефиците окислительно-восстановительных ферментов или их посредников,
возникающем при гормональной недостаточности, а также при повреждении
митохондриальных мембран. К тканевой гипоксии как критическому состоянию
приводит любой вид неустойчивой гипоксии.
Гипоксию можно рассматривать как одну из разновидностей
стрессорных состояний и в соответствии с законом Селье следует ожидать три фазы
ответа организма на стресс.
Первая фаза (возбуждение). Наблюдается усиление
активности окисления первичного субстрата и увеличение продукции АТФ. Этой фазе
соответствует усиление функциональной активности клеток, в частности
интенсификация обменных процессов, в том числе ионного обмена. Происходит
мобилизация функций жизненно важных органов. Повышается сократительная
активность миокарда, частота сердечных сокращений, артериальное давление.
Усиливающуюся гипоксию тканей сердце пытается скомпенсировать увеличением
скорости доставки свежих порций крови на периферию. Повышается ответственность
за управлением всеми функциями организма со стороны мозга, поэтому растет
импульсная активность нейронов, увеличивается частота дыхания. Происходит
экстренный выброс гормонов для мобилизации организма к стрессу, в первую очередь
для усиления доставки тканям энергетического субстрата. Мобилизуются функции
печени для переработки возрастающих потоков недоокисленных метаболитов.
Длительность фазы возбуждения определяется продолжительностью гипоксического
воздействия и интенсивностью его проявления. Эти процессы определяют суть
тренировочного воздействия.
Фаза возбуждения сменяется фазой адаптации. Из-за
ограниченности поступления кислорода в ткани происходит постепенное увеличение
доли восстановленных форм дыхательных ферментов и ингибирование комплекса I
дыхательной цепи. При этом возрастает доля восстановленной формы убихинона –
убихинола. Последний является активатором сукцинатдегидрогеназного комплекса. В
результате происходит переключение субстратного участка дыхательной цепи с
комплекса I на комплекс II, а в клетке начинают накапливаться НАД-зависимые
субстраты цикла Кребса. В этот период, несмотря на нарушение работы комплекса I
за счет скомпенсированной работы комплекса II, внутриклеточная концентрация АТФ
сохраняется неизменной или почти неизменной. При сохранении энергетического
гомеостаза функциональная активность клеток также не меняется. Начальный период
гипоксии, в течение которого сохраняется состояние энергетического гомеостаза в
клетках, относится к компенсированной стадии биоэнергетической гипоксии.
По мере развития гипоксии и снижения запасов кислорода в
тканях наблюдается переход к заключительной фазе реакции организма на стресс –
фазе истощения. На этой фазе можно выделить два последовательно
проходящих этапа деградации электронтранспортных функций митохондрий. На первом
этапе наблюдается подавление биоэнергетических функций дыхательной цепи в
области комплекса III. Этот период соответствует началу нескомпен-сированных
изменений и сопровождается снижением содержания макроэргов в клетках.
Нарушение энергетического гомеостаза – событие с далеко
идущими последствиями для клеток. По этой причине в экстренном порядке
мобилизуются внутренние резервы для ликвидации энергетического дефицита.
Осуществляется запуск запасной биоэнергетической системы – системы анаэробного
окисления субстрата. Происходит централизация кровообращения, при которой не
"отключаются" от перфузии только сердце, головной мозг и почки – основные
жизненно важные системы.
Включение процессов гликолиза происходит в тот момент,
когда в клетке снижается содержание АТФ и увеличивается концентрация АДФ и АМФ.
Клетка переходит в новое нестабильное состояние и возникает реальная угроза для
ее существования. Дальнейшая судьба клетки зависит от энергетических и
субстратных потоков, а также от ряда биохимических и биофизических процессов,
которые в экстренном порядке запускаются по мере дизэнер-гизации клетки.
По мере развития гипоксии наблюдается поэтапное повреждение
элементов дыхательной цепи. После последовательного подавления переноса
электронов через комплексы I, II и III в дыхательной цепи сохраняется последняя
возможность образования АТФ за счет работы цитохромоксидазы (комплекса IV). Но в
условиях усиливающейся гипоксии и дезорганизации работы многих ферменных систем
сохранивший работоспособность фрагмент дыхательной цепи уже не способен
удовлетворить энергетические запросы клетки. Этому обстоятельству способствует
также относительный и абсолютный субстратный дефицит. Как известно, субстрат для
комплекса IV – восстановленная форма фермента цитохрома С. Последняя окисляется
кислородом с помощью цитохромоксидазы и превращается в окисленную форму
фермента. При инактивации комплекса III, в котором обычно осуществлялось
ферментативное восстановление окисленной формы фермента, наступает относительный
субстратный дефицит. В этих условиях клетка использует запасные механизмы
восстановления фермента за счет реакций не ферментативного взаимодействия
последнего с убисемихиноном или супероксидным ион-радикалом. Таким образом
удается восстановить поставку субстрата для комплекса IV, нарушенную в
результате инактивации в комплексе III.
Однако относительный субстратный дефицит вскоре сменяется
на абсолютный. Последнее обстоятельство связано с повреждением мембранных
структур. По мере поэтапного выключения в условиях гипоксии отдельных комплексов
дыхательной цепи наблюдается последовательное снижение сопрягающих функций
митохондрий. Открываются протонные каналы во внутренней мембране митохондрий,
что обеспечивает на время поступление свежих партий макроэргов. И за их
появление приходится платить все более дорогую цену. В результате набухания
митохондрий и дальнейшего увеличения размера пор из матрикса в цитоплазму клетки
перемещаются различные субстраты и низкомолекулярные белки, включая цитохром С.
Потере последнего способствует снижение мембранного потенциала на
митохондриальной мембране. Как известно, молекула фермента имеет избыточный
положительный заряд и удерживается на внутренней стороне митохондриальной
мембраны преимущественно за счет электростатических сил притяжения. По мере
снижения величины мембранного потенциала молекулы цитохрома С начинают покидать
поверхность мембраны и комплекс IV лишается своего субстрата. Дыхательная
активность в этом случае полностью подавляется, и клетка гибнет.
Антигипоксэнты
Антигипоксантами называют средства, улучшающие усвоение
организмом кислорода и снижающие потребность органов и тканей в кислороде, тем
самым способствующие повышению устойчивости организма к кислородной
недостаточности.
Исследования убедительно свидетельствуют, что наиболее
перспективны в борьбе с гипоксией в спорте фармакологические средства,
воздействующие на митохондриальные комплексы (табл. 12-14).
Условно антигипоксанты могут быть разделены на группы:
– препараты непосредственно антигипоксического действия;
– корригирующие метаболизм в клетке:
• мембранопротекторного действия,
• прямого энергизирующего действия (влияющие на
окислительно-восстановительный потенциал клетки, цикл Кребса и комплексы
дыхательной цепи митохондрий);
– действующие на транспортную функцию крови:
• повышающие кислородную емкость крови,
• повышающие сродство гемоглобина к кислороду,
• вазоактивные вещества эндогенной и экзогенной природы.
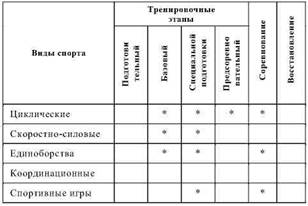
Биоэнергетическое воздействие отдельных препаратов на коплексы митохондриальной дыхательной цепи
Применение антигипоксантов
Антигипоксанты
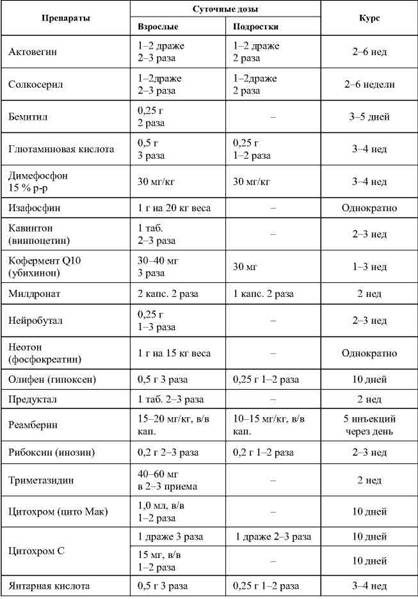
Примечание. Применяется один из представленных в таблице препаратов, оказывающий максимальное действие с минимальными осложнениями и побочными эффектами.
Олифен (гипоксен). Антигипоксант. Механизм
действия олифена на клетки заключается в снижении потребления тканями кислорода,
его более экономном расходовании в условиях гипоксии.
Олифен – фермент дыхательной цепи синтетической природы.
Обладая высокой электронно-обменной емкостью за счет полифе-нольной структуры
молекулы, олифен оказывает шунтирующее действие на стадии образования молочной
кислоты из пировино-градной кислоты, образуя ацетил Ко А, который затем
вовлекается в цикл трикарбоновых кислот. Олифен на молекулярном уровне облегчает
тканевое дыхание в условиях гипоксии за счет способности непосредственно
переносить восстановленные эквиваленты к ферментным системам. Препарат
многократно компенсирует недостаток убихинона в условиях гипоксии, так как
содержит большое количество функциональных центров. Таким образом, олифен
компенсирует деятельность митохондриальной дыхательной цепи при наличии
повреждений на ее участках.
Антиоксидантное действие олифена связано с его
полифеноль-ной структурой, которая защищает мембраны клеток и митохондрий от
разрушительного воздействия свободных радикалов, образующихся в процессе
перекисного окисления липидов. Этот патологический процесс запускается при
экстремальных физических и психоэмоциональных воздействиях на организм.
Олифен улучшает переносимость гипоксии за счет увеличения
скорости потребления кислорода митохондриями и повышения сопряженности
окислительного фосфорилирования.
Будучи препаратом прямого действия, может обеспечить
кислородом любую клетку за счет малых размеров собственных молекул. В связи с
этим его применение возможно при всех видах гипоксии.
Экономное расходование энергетических запасов происходит за
счет переведения с гликолитического на аэробное окисление энергетических
субстратов, т е. на более выгодный механизм обмена. При этом выход энергии
увеличивается в 19 раз, так как при анаэробном гликолизе одной молекулы
получается 2 молекулы АТФ, а при аэробном – 38 молекул АТФ.
Водорастворимый антиоксидант, обладая высокой
энергетической емкостью, ставит большое количество электронных ловушек.
Окислительно-восстановительный потенциал олифена – 680, коэнзима Q10 – 122.
Показания к применению в спорте: повышение
работоспособности при выполнении мышечной работы в экстремальных условиях
соревнований; экономное расходование кислорода тканями в условиях гипоксии;
профилактика и преодоление состояния хронической усталости; ускорение
восстановления организма после перенесенных нагрузок; улучшение периферического
кровотока.
Выводится из организма через 6-8 часов.
Побочное действие практически не встречается. В редких
случаях возможна тошнота, сухость во рту.
Олифен улучшает усвоение других веществ (лекарств,
витаминов) на 25%.
Убихинон (кофермент Q-10, коэнзим Q10) –
вещество, которое вырабатывается организмом и поступает с пищей. Оно обнаружено
в говядине (особенно во внутренних органах – сердце, печени, почках), жирной
рыбе, шпинате, арахисе и цельных зернах. Несмотря на то что коэнзим Q10 (CoQ-10)
можно найти во многих свежих продуктах, он неустойчив и легко разрушается
окислением при переработке и приготовлении продуктов.
CoQ-10 участвует в работе электронтранспортной дыхательной
цепи митохондрий. Уменьшает повреждение ткани, вызванное гипоксией, генерирует
энергию и повышает толерантность к физическим нагрузкам. Как антиоксидант
замедляет процесс старения (нейтрализует свободные радикалы, отдавая свои
электроны). Укрепляет иммунную систему.
Наш организм может вырабатывать CoQ-10, если получает в
необходимом количестве витамины В2 , В3 , В6 , С, фолиевую
и пантотеновую кислоты. В случае нехватки любого из этих витаминов синтез CoQ-10
подавляется.
Не имеет токсичных доз и побочных эффектов.
CoQ-Ю принимается в дозировке от 30 до 100 мг в день.
Никотинамид. Амид никотиновой кислоты и
сама никотиновая кислота (витамин РР, ниацин, витамин В3 ), являясь
простетической группой ферментов НАД и НАДФ и переносчиками водорода, участвуют
в процессах тканевого дыхания, метаболизме жиров, углеводов, аминокислот.
Цитохром С (цито Мак). Гемопротеид,
катализатор клеточного дыхания. Стимулирует окислительные реакции и активизирует
тем самым обменные процессы в тканях, уменьшает гипоксию тканей при различных
патологических состояниях. Эффект наступает через несколько минут после в/в
введения и продолжается несколько часов.
При применении возможны аллергические реакции.
Предрасположенным к аллергическим реакциям рекомендуется проводить пробу с
введением 0,5-1 мл цитохрома С, разбавленного 1:10; или 0,1 мл внутрикожно.
Реамберин. Раствор (1,5%) для инфузий
представляет собой хорошо сбалансированный полиионный раствор с добавлением
янтарной кислоты, содержащий: натрия хлорида 6,0 г, калия хлорида 0,3 г, магния
хлорида 0,12 г, натриевой соли янтарной кислоты 15 г, воды для инъекций до 1
литра. Сбалансированный препарат с осмолярностью, приближенной к нормальной
осмолярности плазмы крови человека.
Основной фармакологический эффект препарата обусловлен
способностью усиливать компенсаторную активацию аэробного гликолиза, снижать
степень угнетения окислительных процессов в цикле Кребса, в дыхательной цепи
митохондрий с увеличением внутриклеточного фонда макроэргических соединений (АТФ
и креатин-фосфата). Сукцинат натрия (янтарная кислота) по клинической
классификации относится к субстратным антигипоксантам. Включаясь в
энергетический обмен как субстрат, соли янтарной кислоты направляют процессы
окисления по наиболее экономичному пути.
Реамберин оказывает гепатозащитное действие, уменьшая
продолжительность процессов перекисного окисления липидов и препятствуя
истощению запасов гликогена в клетках печени.
Максимальный уровень концентрации препарата в крови при
внутривенном введении наблюдается на первой минуте после введения. Через 40 мин
его концентрация возвращается к значениям, близким к фоновым.
Инозин (рибоксин). Действие инозина
антигипоксическое, антиаритмическое, анаболическое. Повышает активность ряда
ферментов цикла Кребса и энергетический баланс. Оказывает положительное влияние
на обменные процессы в миокарде – увеличивает силу сокращений и способствует
более полному расслаблению миокарда в диастоле (связывает ионы кальция, попавшие
в цитоплазму в момент возбуждения клетки), в результате чего возрастает ударный
объем; улучшается кровоснабжение тканей, в том числе коронарное кровообращение.
Используется для профилактики метаболических нарушений в
миокарде при экстремальных физических нагрузках, при дистрофии миокарда на фоне
тяжелых физических нагрузок, нарушениях сердечного ритма, для профилактики
заболеваний печени.
При применении возможны тахикардия, обострение подагры,
гиперемия и зуд кожи, другие аллергические реакции.
Актовегин (солкосерил) . Препарат
биологического происхождения. Активирует клеточный метаболизм путем увеличения
транспорта и накопления глюкозы и кислорода, усиления внутриклеточной
утилизации. Улучшает трофику и стимулирует процесс регенерации.
Милдронат. Улучшает метаболические
процессы. Повышает работоспособность, уменьшает симптомы психического и
физического перенапряжения; обладает кардиопротекторным и регулирующим систему
клеточного иммунитета действиями; устраняет функциональные нарушения в
соматической и вегетативной нервной системах. Препарат вызывает уменьшение
содержания свободного кар-нитина, снижает карнитинзависимое окисление жирных
кислот.
Биодоступность – 78%. Максимальная концентрация в плазме
достигается через 1 –2 часа после приема. Период полувыведения – 3-6 часов.
Используется для восстановления после тренировочной и
соревновательной нагрузки; физическом перенапряжении, перетренированности.
В редких случаях возможен кожный зуд, диспептические
явления, тахикардия, возбуждение, изменения АД.
Применять осторожно при тахикардии и гипотензии.
Кавинтон (винпоцетин) . Препарат, улучшающий
мозговое кровообращение и процессы метаболизма в мозговой ткани; способствует
транспортировке кислорода к тканям вследствие уменьшения сродства к нему
эритроцитов, усиливая поглощение и метаболизм глюкозы; уменьшает повышенную
вязкость крови, улучшает микроциркуляцию. Метаболизм глюкозы переключается на
энергетически более выгодное аэробное направление. Стимулирует также и
анаэробный метаболизм глюкозы.
Назначается в случае острой и хронической недостаточности
мозгового кровообращения (транзиторная ишемия в видах спорта на выносливость);
посттравматической и гипертензивной энцефалопатии (травмоопасные виды спорта);
для уменьшения нарушений памяти; при головокружении; головной боли; двигательных
расстройствах.
Антигипоксическим эффектом обладают также витамины С и Е,
адаптогены, ноотропы, оксибутират лития, лимонная и фумаровая кислоты.
При
комбинированном применении антигипоксантов происходит усиление их действия
Возможные комбинации антигипоксических препаратов
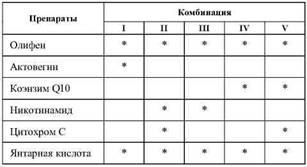
Гипоксическая гипоксия возникает при снижении р02
в легочных альвеолах, крови, клетках тканей, что чаще всего наблюдается при
расстройстве системы внешнего дыхания (заболевания легких, бронхов; слабость
дыхательных мышц, диафрагмы и т. п.) или при подъеме на высоту, в горах.
Тренировка дыхательных мышц и устойчивости к повышенному
количеству углекислого газа (С02 ) в организме возможна с помощью
дыхательных тренажеров.
Гипоксическая тренировка проводится как самостоятельная (на
тренажере) и как дополнение к основной тренировке в виде серии задержек дыхания
с интервалом 1-3 мин (после основной тренировки). То же относится к специальной
подготовке при планировании тренировок в горах.
Поиск путей совершенствования системы подготовки
спортсменов высокой квалификации к соревнованиям привел к методике тренировки в
горных условиях как дополнительному средству повышения спортивной
работоспособности. Подготовка спортсмена в горах подразумевает определенный
сдвиг физиологических констант организма.
По степени воздействия выделяют:
низкогорье – 1000—1400 м над уровнем моря;
среднегорье – до 2500 м;
высокогорье – до 4500 м;
снежное высокогорье – выше 4500 м над уровнем моря.
Обычно горные условия используют с целью:
– выступления на соревнованиях на аналогичной высоте;
– выступления в серии соревнований, проводящихся на разных
высотах;
– повышения спортивных достижений при спуске на равнину.
Чаще всего горную подготовку применяют с последней целью.
Низкогорье (предгорье) эффективно после возвращения на
равнину, главным образом, не за счет адаптации к гипоксическому фактору, а в
связи с воздействием комплекса климатических модификаторов, характерных для этих
высот.
Высокогорье, кроме значительно сниженного атмосферного
давления и парциального давления кислорода, воздействует на состояние спортсмена
перепадом температур, пониженной влажностью.
Для получения эффекта горной подготовки используют в
основном среднегорье.
Среднегорье предъявляет повышенные требования к
функционированию организма спортсмена вследствие изменения парциальных давлений
газов атмосферы. Атмосферное давление снижается по мере возрастания высоты, но
процентное соотношение газов в воздухе остается постоянным. Воздух всегда
содержит 20,94% кислорода, 0,03% углекислого газа, 78,08% азота, 0,94% аргона и
0,01% других газов. Давление, которое производят молекулы кислорода,
непосредственно связано с плотностью атмосферы. Изменение давления кислорода
напрямую влияет на циркуляцию кислорода между легкими и кровью и между кровью и
клетками тканей.
По определению максимальное потребление кислорода
соответствует возможности организма его получить, переработать и использовать.
Диффузия кислорода в кровь зависит от р02 в альвеолах легких, которое
снижается по мере набора высоты, приводя к уменьшению насыщения крови
оксигемоглобином. На уровне моря оксигемоглобин составляет 98%, но каждые 400 м
он падает на 1%.
На уровне моря перепад р02 в крови и клетках тканей
– 74 мм рт. ст. (94 мм рт. ст. – р02 в артериальной крови, 20 мм рт.
ст. – в клетках тканей). Этот перепад – основной фактор, отвечающий за насыщение
тканей кислородом. На высоте около 7000 м перепад очень незначительный и,
следовательно, ткани почти перестают "дышать". Но, например, на уровне 2400 м р02
в крови (артериальной) составляет около 60 мм рт. ст., в то время как в клетках
оно остается на уровне 20 мм рт. ст. Разница составляет только 40 мм рт. ст., т
е. спад в насыщении тканей кислородом на этой высоте составляет около 50%.
По мере того как р02 падает, стимулируется
вентиляция легких. Это вызывает повышенное выделение С02 и респираторный
алкалоз. Выделяется и остается на низком уровне бикарбонат, снижается буферная
емкость, повышается рН крови.
Поглощение кислорода клетками мышц на высоте снижается, но
после продолжительного пребывания в этих условиях немного увеличивается. В
организме возникает ряд защитных компесаторно-приспособительных реакций. В
первую очередь недостаток 02 приводит к возбуждению хеморецепторов. Их
возбуждение служит сигналом для углубления и учащения дыхания. Увеличивается
альвеолярная поверхность, что способствует более быстрому насыщению гемоглобина
кислородом. К тому же гипоксия, которая усиливается во время напряженной работы
на высоте, мешает тренироваться с адекватной интенсивностью и в нужном объеме.
Так как
кислородные возможности на высоте ограничены, то при любой заданной рабочей
нагрузке выработка молочной кислоты выше, чем на уровне моря. Сердечная
деятельность на высоте усиливается, пытаясь компенсировать сокращенное питание
тканей кислородом. Таким образом создаются условия для перенапряжения сердечно-сосудистой и центральной нервной систем. Вторично страдают насыщенные сосудами органы.
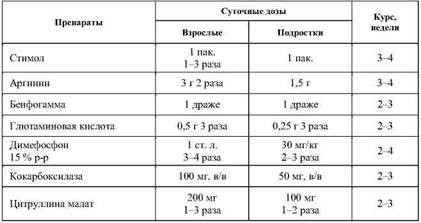
Фармакологическую коррекцию необходимо начинать за 10-12 дней до дня переезда. Препараты железа, магния в профилактических дозах. Адаптогены. Иммунокорректоры. Для профилактики сердечно-сосудистых осложнений назначаются препараты, улучшающие реологические свойства крови, обменные процессы в сердечной мышце. Анаболические средства – оротат калия, магнерот, трибулус, левзея, флавостен. Улучшающие усвоение глюкозы и кислорода: янтарная кислота, глютаминовая кислота, коэнзим Q-10. Витамины – суточная потребность в большинстве из них в горах возрастает в 1,5-2 раза. Углеводы (преимущественно в виде напитков) – спортивные напитки, напитки из фруктозы, меда (насыщение во время тренировок).
Фармакологическая поддержка во время тренировок в горах должна соответствовать этапу подготовки.
Фармакотерапия после спуска на "равнину" должна быть направлена на повышение функциональных возможностей спортсмена и предупреждение срыва процессов реадаптации. Необходимо продолжить применение препаратов, улучшающих микроциркуляцию и реологические свойства крови. Адаптогены назначаются в половинной дозе от той, что применялась в горах. Следует усилить витаминизацию, обращая особое внимание на витамин Е, обладающий антиоксидантными свойствами, предотвращающий быстрое разрушение эритроцитов. Необходимо также поддержать функцию сердца, печени, почек.
При возвращении на равнину первые 7 дней ("острый период") идет процесс реадаптации с ухудшением спортивных результатов и риском возникновения заболеваний (особенно 3-4-й день); далее следует подъем работоспособности. Пик результативности (индивидуален по срокам) возможен на 18-30-й день. Молодые спортсмены без горного стажа в процессе адаптации более сильно реагируют на тренировочные нагрузки, что удлиняет сроки "острой" акклиматизации. Благоприятно влияют на адаптацию горный стаж и степень подготовленности спортсмена.
Гемическая гипоксия. Гемоглобин (hb) в
эритроцитах – средство доставки кислорода и удаления углекислого газа из тканей.
Повышение кислородной емкости крови за счет увеличения уровня Hb – один из
способов коррекции гипоксии. Hb, состоящий из гема и глобина, для своего
образования в качестве пластического материала требует железо, аминокислоты,
витамины (цианкобаломин, фолиевая кислота и др.).
Кроме Hb железо присутствует в миоглобине миофибрилл мышц,
участвует во множестве биохимических реакций как катализатор.
Дефицит железа в организме возможен при: недостатке железа
в пищевом рационе; нарушении усвоения железа; при повышенных потерях железа с
потом, мочой; перераспределении белка, железа в пользу рабочей гипертрофии мышц;
физиологических потерях Hb у спортсменок.
Кроме того, возможно относительное снижение концентрации Hb
в крови за счет увеличения объема циркулирующей плазмы, т е. разведения его в
большем объеме.
Истощение запасов железа в организме спортсмена приводит:
а) к снижению уровня физической работоспособности за счет:
– эргометрических показателей,
– изменения газовых градиентов организма (кислорода и
углекислоты),
– накопления молочной кислоты;
б) к перетренированности.
Контроль Hb в циклических видах спорта необходимо
осуществлять ежемесячно. Для выявления скрытого дефицита железа используются
углубленные методы исследования.
Коррекция должна начинаться сразу после выявления дефицита
железа:
1) возмещение дефицита железа в крови и тканях препаратами;
2) восстановление метаболизма в эритроцитах и других
клетках;
3) коррекция причин, лежащих в основе дефицита железа.
Мероприятия проводятся до нормализации состояния
спортсмена, полного восстановления как Hb (минимум 140 г/л), так и "железа
запасов" (уровень ферритина) с помощью витаминизации и приема анаболических
препаратов растительного происхождения, антиоксидантов. В начале цикла
подготовки спортсмена к соревнованиям необходимо провести несколько курсов для
создания достаточных запасов железа. Женщинам проводят два курса базовой
профилактики в течение сезона.
Предпочтение следует отдавать тем препаратам, которые
наряду с железом содержат минералы, способствующие лучшему его усвоению.
Хорошей антианемической активностью обладают: актиферрин,
конферон, сорбифер дурулес, тотема, фенюльс, ферретаб, феррокаль, ферроплекс,
феррофольгамма; препараты с пролонгированным действием: ферроградумет,
тардиферон, ферроград 500.
Тотема. Комбинированный препарат,
содержащий микроэлементы: железо в виде глюконата, марганец, медь.
Железо, входящее в состав препарата, быстро восполняет
нехватку этого элемента в организме, стимулирует эритропоэз. После курса
препарата происходит постепенная регрессия клинических (слабость, утомляемость,
тахикардия) и лабораторных симптомов анемии. Марганец и медь являются важной
составной частью ферментативных систем, участвующих в основных
окислительно-восстановительных процессах в организме.
Показания в спорте: повышенное потребление железа
при физической нагрузке, недостаточное поступление железа с пищей, повышенная
потеря железа на тренировках и соревнованиях при неблагоприятных условиях,
профилактика железодефицитной анемии у спортсменов из группы повышенного риска,
лечение железодефицитной анемии.
Применение. Содержимое ампул растворяют в воде (с
сахаром или без) или в любой другой питьевой жидкости, не содержащей спирт.
Желательно принимать препарат натощак. В процессе лечения время приема препарата
и режим дозирования корректируют в зависимости от индивидуальной переносимости
пациента (возможного побочное действие со стороны ЖКТ).
В профилактических целях назначают 50 мг элементарного
железа в сутки в течение 1-3 месяцев.
Детям назначают по 5-10 мг на кг массы тела элементарного
железа в сутки.
Взрослым для лечения анемии: 100—200 мг элементарного
железа в сутки. Срок лечения зависит от исходного уровня Hb и соответствует 1-2
месяцам. При необходимости препарат может применяться более длительное время.
Установлено, что избыточное потребление чая подавляет
всасывание железа. При курсовом применении препарата возможно окрашивание кала в
черный цвет.
Контроль лабораторных показателей: уровень
гемоглобина, количество эритроцитов, цветовой показатель, средний объем
эритроцитов, содержание железа в сыворотке крови.
Нарушение процессов адаптации к физическим нагрузкам со
стороны крови может сопровождаться появлением жалоб, функциональными
расстройствами со стороны внутренних органов (висцеропатии): нарушением
процессов реполяризации в сердечной мышце, дискинезией желчевыводящих путей,
доброкачественной гипербилирубинемией, гиперферментемией, ЛОР-заболева-ниями.
Обоснованными методами лечения при наличии висцеропатии,
обусловленных дефицитом железа, считаются комплексное использование
эссенциальных фосфолипидов, кислородсберегающих метаболических средств
(милдронат, предуктал), мембраностаби-лизаторов на фоне базисной терапии
ферропрепаратами и антиок-сидантами. Срок лечения зависит от исходного уровня
гемоглобина и соответствует 1-2 месяцам.
При сохраняющемся дефиците железа проведение курсами
поддерживающей терапии продолжается.
Сохранение параметров красной крови гарантирует оптимальное
функционирование всей системы кислородного транспорта.
При исседовании показателей красной крови ориентируются на
уровень гемоглобина, количество эритроцитов, ретикулоцитов, гематокрит, железо
сыворотки, а также возраст эритроцитов.
Эритроциты – не однородная масса клеток. Они образуют
по-пуляционную систему, в которой закономерно сочетаются клетки различного
состояния. Эритроциты характеризуют размер (объем), количество в них
гемоглобина, стойкость мембран. Разрушение и последующая "утилизация" эритроцита
происходит после исчерпания им своих функциональных возможностей или в
результате повреждающих патогенных факторов.
Длительность жизни эритроцитов в среднем составляет 110—120
дней и чаще всего зависит от количества контактов гемоглобина с кислородом и
стойкости эритроцитарной оболочки.
Под влиянием физической нагрузки возраст эритроцитов может
меняться как в сторону старения, так и в сторону омоложения.
По стандартной методике принято разделять эритроциты на три
группы по функциональному состоянию и стойкости по отношению к внешним
повреждающим факторам, что в норме соответствует (по мере созревания) трем
возрастным группам эритроцитов.
Эритрограмма дает представление о физиологическом возрасте
эритроцитов.
Молодые эритроциты (юные) – возраст до 28-30 дней.
Содержание в норме 20-25%. Группа особо стойких эритроцитов.
Зрелые эритроциты – возраст 30-90 дней. Содержание
в норме 45-55% всех клеток. В этом статусе эритроцит проводит большую часть
жизни. Зрелые эритроциты наиболее полно участвуют в транспорте и обмене
кислорода.
Эритроциты, возраст которых больше 90 дней (20-25%), –
группа низкостойких эритроцитов.
Под влиянием физических нагрузок могут происходить
изменения в характере эритрограммы в виде смещения максимума по группам.
Сдвиг максимума эритроцитов в сторону физиологического
старения может быть связан с физическим переутомлением, угнетающим процессы
эритропоэза.
Сдвиг максимума эритрограммы в сторону омоложения
эрит-роцитарного состава крови (связан с стимуляцией процесса эритропоэза)
указывает на адекватность предложенных тренировочных нагрузок.
Резкое снижение количества зрелых эритроцитов обусловлено
понижением резистентности эритроцитарных мембран, что встречается при
несоответствии физической нагрузки функциональному состоянию организма
спортсмена.
Наличие в кровяном русле эритроцитов нескольких групп с
резко различными свойствами (на эритрограмме отчетливо проявляются несколько
максимумов) свидетельствует о глубоких нарушениях равновесия системы крови
(характерно для перетренированности).
Наиболее адекватная реакция на предлагаемую физическую
нагрузку – нормальное (без сдвига) сочетание количества эритроцитов всех
возрастов или некоторое омоложение эритроцитарно-го состава крови.
Имеется индивидуальная склонность к явлениям старения или
омоложения эритроцитов на протяжении тренировочного "сезона".
Количество эритроцитов в крови и содержание гемоглобина в
них зависят от вида спорта, разряда (спортивных достижений), уровня
тренированности, места проживания и пола спортсмена (Макарова Г.А., 1990).
Учет резервов системы красной крови позволяет адаптировать
организм спортсмена к продолжительным, интенсивным нагрузкам, поддерживать
оптимальное функционирование всей системы кислородного транспорта.
3. Кислотно-основное состояние и ионное равновесие
В практике спортивной медицины контроль за эффективностью
тренировочного процесса осуществляется на основе оценки комплекса параметров,
среди которых определенная роль отводится показателям кислотно-основного
состояния (КОС). Эти показатели – объективные критерии подготовленности
спортсменов, они могут быть использованы для выявления уровня энергообеспечения
мышечной деятельности, функционального состояния сердечно-сосудистой и
дыхательной систем, адаптации к спортивной нагрузке.
Причинами нарушений КОС и ионного равновесия в организме
при физической нагрузке могут быть длительная работа в гликолитическом режиме,
анемия, недостаток бикарбонатов.
Как следствие измененяется буферная емкость крови,
происходит накапливание молочной кислоты (La), сдвиг рН крови в кислую сторону
(ацидоз). Решающую роль играет скорость увеличения концентрации молочной
кислоты. Итогом запаздывания утилизации La становится резкое снижение физической
работоспособности спортсмена.
Для выявления и контроля могут быть использованы: La, pH,
Hb в крови. Эти показатели – объективные критерии подготовленности спортсмена и
его адаптации к спортивной нагрузке.
Необходимая коррекция должна быть направлена на увеличение
буферной емкости крови, ощелачивание, снижение уровня молочной кислоты,
сохранение водно-солевого баланса.
Динамика кислотно -основного состояния
Кислотно-основное состояние (КОС) – один из основных
показателей, характеризующих функционирование организма человека как единого
целого. Его иногда не совсем правильно называют "кислотно-щелочное равновесие"
(КЩР). На самом же деле организм только стремится к этому равновесию, сохраняя
постоянство внутренней среды – гомеостаз.
Изменения КОС в большей степени связаны с изменениями
водно-электролитного равновесия. Известно, что в живом организме все жидкости
являются электронейтральными и подчиняются физико-химическим законам, т е. сумма
положительно заряженных частиц (катионов) равна сумме отрицательно заряженных
частиц (анионов). Динамическое нарушение электронейтральности, постоянно
возникающее в организме, немедленно отражается на КОС и быстро ликвидируется.
КОС – это состояние, которое определяется соотношением
между водородными и гидроксильными ионами. Истинная кислотность зависит от
активности и концентрации ионов водорода (Н+ ), а щелочная реакция
(реакция основания) – от концентрации ионов гидроксила (ОН-). Концентрацию ионов
водорода называют водородным показателем рН (рН нейтрального раствора равен 7,
рН кислого раствора < 7, рН щелочного раствора > 7).
В здоровом организме рН колеблется в узких пределах –
7,35-7,45 за счет постоянного образования в процессе обмена веществ щелочных и
кислотно-реагирующих соединений.
Регуляторными системами, обеспечивающими это постоянство,
являются буферные системы: бикарбонатная, гемоглобиновая, фосфатная, а также
белки сыворотки крови. Большое значение в этих процессах имеет выделение
углекислого газа (С02 ) легкими. Парциальное давление углекислого газа
крови (рС02 ) – фактически единственный показатель дыхательной части КОС.
Внутреннюю среду организма как единого целого характеризуют
физические и биохимические константы:
– реакция рН, отражающая КОС;
– стандартный бикарбонат (SB) – обменный фактор, который
служит для нейтрализации поступающих в кровь кислот (мэкв/л);
– остаток кислот (BE) – показатель, по которому оценивается
степень метаболического ацидоза (мэкв/л);
– рС02 – дыхательный фактор, служит мерой оценки
первичных нарушений и вторичных компенсаторных реакций.
Принято считать:
рН 7,40-7,35 – компенсированный ацидоз (закисление);
рН 7,34-7,28 – субкомпенсированный ацидоз;
рН 7,27 и ниже – декомпенсированный ацидоз.
За норму приняты следующие величины показателей КОС:
рН 7,36-7,42;
SB 21,3-25,7;
BE –2,4 … +2,4;
pC02 35,0-45,0.
Возрастание этих величин – алкалоз; уменьшение – ацидоз.
Сдвиг показателей рН, BE, pC02 за нижнюю границу
свидетельствует о возникновении метаболического ацидоза. Нарастание
метаболического ацидоза отражает неадекватную доставку кислорода тканям при
значительном увеличении потребления кислорода.
При изменении КОС защитные механизмы начинают действовать
немедленно. Первыми включаются буферные системы, нейтрализующие действие избытка
кислот или оснований. Второй системой защиты служат легкие и почки, причем
легочный механизм более мобильный.
Важнейшим условием диагностики и коррекции изменений КОС
должно быть определение первичности нарушений. Любое изменение КОС
сопровождается компенсацией, т е. метаболический ацидоз может компенсироваться
дыхательным алкалозом или метаболический алкалоз – дыхательным ацидозом.
Парциальное давление углекислого газа (рС02 ).
Нарастание рС02 крови вызывает немедленную стимуляцию дыхания и
увеличение альвеолярной вентиляции, что нормализует рС02 . Понижение рН
при метаболическом ацидозе раздражает С02 – рецепто-ры. Благодаря
гипервентиляции возникает дыхательный алкалоз и рН возвращается к норме. рС02
в артериальной крови при очень больших нагрузках несколько снижается, причем у
спортсменов чуть меньше, чем у неспортсменов, что связано с более совершенной
регуляцией дыхания у спортсмена.
Стандартный бикарбонат (SB). Буферные основания
крови – важнейшие механизмы в регуляции КОС. В условиях покоя содержание SB в
крови у спортсменов в среднем такое же, как у нетренированных – соответственно
24,3 и 24,4 мэкв/л. Однако снижение содержания SB у спортсменов происходит при
более значительных нагрузках, чем у неспортсменов. Это объясняется различиями в
изменении концентрации La в крови: у спортсменов она ниже, чем у неспортсменов.
Остаток кислот (избыток буферных оснований – BE).
Наибольшие сдвиги в кислую сторону отмечены при анаэробных реакциях. При
этом наиболее точную информацию дает величина BE, что позволяет использовать
этот показатель для определения граней аэробно-анаэробного перехода. Правомерно
сопоставление показателя BE с показателем концентрации лактата, что дает
возможность оценить работоспособность спортсмена в данный момент. Для
определения активации анаэробной энергопродукции в работающих мышцах необходимо
определять BE до и после физической нагрузки и анализировать результат. При
использовании только одних абсолютных показателей BE невозможно точно дать
оценку выполненной работы, так как сдвиги КОС крови зависят не только от степени
тренированности и выполненной нагрузки, но и от исходного состояния этих
показателей.
Концентрация водородных ионов (рН) отражает уровень
кислотно-основного состояния организма.
При выполнении одинаковой по мощности нагрузки:
– у тренированного спортсмена рН крови может смещаться до
7,15, а у нетренированных до 7,01;
– у женщин явления ацидоза при одинаково выполненной
нагрузке выражены больше, чем у мужчин;
– у юных спортсменов степень ацидоза больше, чем у
спортсменов старшего возраста.
Однако при выполнении нагрузки максимальной мощности сдвиги
КОС несколько уменьшаются с возрастом. Это связано с тем, что выполнение такой
работы лимитируется функциональными возможностями биологических систем
жизнеобеспечения организма.
При использовании показателей КОС необходимо иметь в виду,
что наибольшая информативность этих показателей характерна для представителей
тех видов спорта, где спортивный результат в значительной мере определяется
уровнем активности механизмов энергетического обеспечения работы и значительной
ролью гли-колитического процесса.
При физической нагрузке увеличивается содержание кислых
продуктов обмена, которые вызывают сдвиги КОС крови. Степень изменений КОС
зависит от длительности и интенсивности физической нагрузки, а также от
функционального состояния организма в целом.
рН крови в наибольшей степени зависит от содержания в ней
La, а также от рС02 и буферных возможностей крови. В состоянии покоя рН
артериальной крови у спортсменов практически такая же, как и у неспортсменов.
Поскольку во время мышечной работы рН почти исключительно определяется
концентрацией молочной кислоты, все что можно сказать об эффектах тренировки по
уровню La крови, справедливо и для рН.
У спортсменов, тренирующих выносливость, снижение рН
происходит при более значительных нагрузках, однако его значение меньше, чем у
нетренированных. Вместе с тем при максимальных аэробных нагрузках снижение рН у
спортсменов больше, чем у неспортсменов. В отдельных случаях рН артериальной
крови у высококвалифицированных спортсменов может падать до 7,0 и даже несколько
ниже.
Следует иметь в виду, что снижение внутриклеточного рН,
вызванное увеличенной концентрацией La, препятствует мышечному сокращению,
снижает способность мышц к поддержанию силы. Накопление кислых продуктов обмена
веществ в процессе напряженной физической работы обусловлено прежде всего
несоответствием между кислородным запросом и его потреблением, что и приводит к
увеличению содержания La в крови и снижению рН.
Сдвиги показателей рН, BE зависят от типа энергообеспечения
мышечной работы. Елубина и напряженность нарушений КОС зависят от уровня
тренированности спортсмена.
Чем тренированнее спортсмен, тем совершеннее механизм
компенсации метаболических нарушений.
Коррекция лактатного метаболизма
Утилизация лактата – достаточно серьезная проблема спорта.
Накопление La в организме во время тренировок и
соревновательной деятельности – один из основных факторов, лимитирующих
повышение работоспособности и результативности спортивных достижений (особенно в
циклических видах спорта).
Накопление La, превышение возможностей организма в его
утилизации и, следовательно, сдвиг рН внутренней среды ("закисление") происходит
при гликолитическом механизме энергообеспечения, связанном с расщеплением
углеводов до La.
Основной путь получения энергии в гликолитическом режиме –
это цикл Кребса (цикл трикарбоновых кислот – ЦТК, цикл лимонной кислоты), т е.
цикл последовательного превращения глюкозы в пировиноградную, лимонную,
глютаминовую, янтарную, муравьиную, яблочную, молочную (La) кислоты с
последующим окислением до С02 и Н2 0. La – конечный продукт,
который, накапливаясь, "закисляет" организм, т е. сдвигает КОС внутренней среды
в кислую сторону.
Непосредственным источником энергии при мышечном сокращении
является расщепление АТФ, богатого энергией соединения. Расходуемые запасы АТФ
должны быть немедленно пополнены, иначе мышцы теряют способность сокращаться.
Восстановление (ресинтез) АТФ осуществляется за счет анаэробных и аэробных
процессов (см. "Энергообеспечение мышц").
Гликолитический механизм энергообеспечения связан с
проявлением так называемой лактатной выносливости. В наибольшей мере этот
анаэробный механизм ресинтеза АТФ проявляется в упражнениях субмаксимальной
интенсивности, продолжающихся от 20-30 с до 2-3 мин. Гликолитические (или
лактатные) возможности организма зависят от запасов углеводов, находящихся в
виде гликогена в мышцах (300—400 г), печени (40-70 г) и в виде свободной глюкозы
в крови и во внеклеточной жидкости (25-30 г).
Определяется гликолитическая емкость по формуле:
Е = ALa х 0,0624 М,
где Е – емкость гликолиза, ALa – максимальная концентрация
молочной кислоты в крови после предельной работы до 2 мин (за вычетом исходного
уровня), 0,0624 – коэффициент пропорциональности для пересчета концентрации La
крови к единице массы (М) спортсмена.
Кроме того, и это особенно важно для спортсмена,
гликолити-ческие возможности зависят от способности организма противостоять
неблагоприятным изменениям в нем в связи с накоплением значительных количеств
La.
Реакция внутренней среды организма сдвигается при этом в
кислую сторону.
Нейтрализация La осуществляется буферными системами и
зависит от их емкости. Буферная емкость крови состоит из бикарбонатной – 13%,
фосфатной – 1%, белковой – 86% (из них 76% приходится на долю гемоглобинового
буфера). Буферные системы крови мало изменяются под влиянием тренировок;
тренируемой считается "способность терпеть", т е. выполнять работу в условиях
неблагоприятных сдвигов в организме, связанных с накоплением продуктов
анаэробного обмена.
Поскольку спортсмен должен в своей деятельности развить
максимальную мощность и по возможности поддерживать ее в течение заданного
времени, изменения во внутренней среде организма происходят в очень короткий
промежуток времени. Фактором, лимитирующим работоспособность спортсмена в этих
условиях, становится не столько величина, сколько скорость накопления продуктов
анаэробного обмена.
Ресинтез (восстановление) La в гликоген происходит в
печени. Этот путь устранения La особенно важен при длительной работе.
Результатом мышечной активности является также накопление
продуктов дезаминирования. Аммиак, который появляется в крови при мышечной
работе, образуется в результате отщепления иона аммония от АМФ.
Этот процесс необходим для полноценного процесса ресинтеза
АТФ из двух молекул АДФ при помощи фермента аденилат-киназы. Накопление аммиака
приводит к усилению образования La. Таким образом, образуется порочный круг,
вызывающий снижение сократительной способности мышц, повреждение структурного
белка – разрушение миофибрилл и, как следствие, дистрофические проявления в
системах и органах, лимитирующих продолжительную (на выносливость)
работоспособность: печени, почках, сердечно-сосудистой, дыхательной,
гематологической системах.
Можно усилить выделение аммиака путем ускорения
использования его в синтезе мочевины.
Здесь доступны два варианта:
а) введение бикарбонатов (например, Na2 C03
4% раствор) для использования С02 в синтезе мочевины (повышение буферной
емкости – бикарбонатной);
б) ускорение оборота цикла синтеза мочевины добавлением
промежуточных продуктов цикла – аминокислот (аргинина, орнитина, цитруллина).
Препараты аминокислот с разветвленными цепями (аргинин,
глютамин, орнитин, цитруллин) уменьшают порог аммиачного блока, нормализуют
аминокислотный состав крови.
Мероприятия, направленные на коррекцию лактатного
метаболизма (табл. 20, 21):
• Уменьшение накопления La посредством введения веществ,
помогающих обойти аммиачный блок (и таким образом разорвать порочный круг).
Такими веществами могут быть: производные янтарной кислоты – сукцинаты (цитрат
натрия), сама янтарная кислота; производные яблочной кислоты – малеаты;
глютамино-вая кислота, лимонная кислота.
• Применение янтарной кислоты, бикарбонатов помогает
снизить скорость накопления продуктов обмена в анаэробном цикле и сохранить
миофибриллы от повреждения.
• Улучшение работы печени препаратами соответствующей
направленности (лецитин, эссенциале, гептрал и т п.) позволяет увеличить
ресинтез La в гликоген.
• Фармакологические формы фосфора, магния, железа
способствуют увеличению буферной емкости крови и, значит, более длительному
сохранению максимальной работоспособности в глико-литическом режиме, а также
более быстрому периоду восстановления. За счет увеличения уровня Hb крови
повышается буферная емкость – гемоглобиновая.
• Усиление протекания метаболических процессов способствуют
микроэлементы, в частности железо, фосфор, магний, кобальт (составные части
энзимов – катализаторов).
• Препараты цинка (цинкит) снижают уровень активности ПОЛ.
Цинк участвует в метаболизме как кофактор многих ферментов, в том числе
ферментов синтеза мочевины.
• Воздействие на пируватдегидрогеназный комплекс
(дихло-рацетат, димефосфон) позволяет увеличить количество АТФ.
• Обеспечение достаточным количеством калорий (глюкоза,
фруктоза, мед) приводит к снижению процессов катаболизма и уровня
гипераммониемии (мочевины) и закисления.
• Энзимы опосредованно увеличивают буферную емкость крови,
уменьшают уровень мочевины.
• Длительное применение гомеопатических средств (ацидум
лактикум, ацидум фосфорикум и т. п.) также позволяет корректировать лактатную
загруженность.
• Массаж, массаж с яблочным уксусом, водные процедуры
ускоряют процесс выведения La из организма.
Ниже даны краткие характеристики препаратов, способствующих
коррекции содержания La.
Применение корректоров лактат-ацидоза
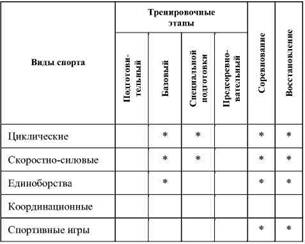
Препараты корректоры лактат-ацидоза
Примечание. Применяется один из представленных в таблице препаратов, оказывающий максимальное действие.
Дихлорацетат обладает способностью
стимулировать активность пируватдегидрогеназного комплекса, что обусловливает
уменьшение образования молочной кислоты и снижения ее содержания в тканях и
биологических жидкостях. Нормализуется КОС. Препарат назначается в дозе 35-50
мг/кг/сут. Продолжительность курса не уточнена. Возможно побочное действие
дихлорацетата – периферическая нейропатия после длительного применения.
Димефосфон – фосфорорганическое соединение,
обладающее способностью усиливать тканевое дыхание и стабилизировать состояние
клеточных мембран. В клинической практике и в эксперименте показано
нормализующее действие димефосфона на равновесие кислот и оснований, уровень
молочной и пировиноград-ной кислот в крови, ПОЛ. В результате активирующего
воздействия димефосфона на пируваткарбоксилазу равновесие между La и пируватом
смещается в сторону последнего, усиливается утилизация пирувата в цикле Кребса,
увеличивается фракция АТФ и повышается отношение АТФ/АМФ. Суточная доза
препарата составляет 30 мг/кг.
Кокарбоксилаза. Кофермент, образующийся в
организме из тиамина (витамина BF).
Оказывает регулирующее воздействие на отдельные функции
организма, главным образом на обменные процессы. Участвует в обмене веществ в
качестве коэнзима; особенно важную роль играет в углеводном обмене. Снижает в
организме уровень молочной и пировиноградной кислот, улучшает усвоение глюкозы.
Нормализует трофику нервной ткани, способствует восстановлению функций
сердечно-сосудистой системы.
Показания: при различных патологических состояниях,
требующих улучшения углеводного обмена, ликвидации дыхательного ацидоза при
легочно-сердечной недостаточности; печеночной и почечной недостаточности;
недостаточности кровообращения, периферических невритах.
Бенфогамма. Действующее вещество препарата
кокарбоксилаза.
Аргинин (незаменимая аминокислота).
Участвует в цикле обмена мочевины, способствует обезвреживанию и выведению из
организма аммиака. Понижает АД. Режим дозирования индивидуальный, в зависимости
от показаний и возраста. В спорте применяют внутрь. С осторожностью применяют
при заболеваниях почек, нарушении обмена электролитов.
Глютаминовая кислота (заменимая
аминокислота). Нормализует обменные процессы, стимулирует окислительные
процессы, способствует нейтрализации и выведению из организма аммиака, повышает
устойчивость организма к гипоксии. Способствует синтезу ацетилхолина и АТФ,
переносу ионов калия. Глютаминовая кислота относится к нейромедиаторным
аминокислотам, стимулирующим передачу возбуждения в синапсах ЦНС.
Применяется при тренировке в гликолитическом режиме
(снижает уровень лактатной загруженности путем разрыва аммиачного блока);
перетренированности (поддержка ЦНС), депрессии. Глютаминовую кислоту применяют
также для снятия нейротоксических явлений, связанных с приемом других
препаратов.
При длительном применении возможно снижение содержания Hb,
лейкопения.
В период применения необходимо проводить исследования мочи
и крови. При возникновении побочных эффектов рекомендуется уменьшение дозы
препарата.
Стимол (цитруллин + малат) – способствует
утилизации La. Препарат расширяет возможности организма спортсмена в тренировках
на выносливость, позволяет отодвинуть границу неблагоприятных ощущений и
"терпеть" их более длительное время, следовательно, увеличить объем и
интенсивность нагрузок.
Применяются также лимонная кислота, натрия гидрокарбонат,
трометамол, цитруллин.
Сохранение водно -солевого баланса
Длительная физическая нагрузка и выраженный дефицит
жидкости могут привести к нарушению электролитного баланса, изменению КОС со
всеми вытекающими негативными последствиями.
При потере жидкости у спортсмена появляются определенные
симптомы:
потеря 1% воды от общего веса вызывает чувство жажды;
2% – снижение выносливости;
3% – снижение силы;
5% – снижение слюноотделения и мочеобразования, учащенный
пульс, апатия, мышечная слабость, тошнота.
Выполнение нагрузок на максимальном уровне потоотделения
может привести к общей потере до 5-6 л жидкости.
При форсированной сгонке веса (применение мочегонных
средств, тепловых процедур, ограничение жидкости) спортсмен может снизить вес на
3-4 кг за 1-2 дня (в несколько приемов), что не исключает потоотделение во время
соревнований. Это приводит к состоянию обезвоживания организма так же, как при
тренировке в горах, в условиях жаркого климата и даже в невентилируе-мых залах
летом. Как следствие, происходит значительное снижение аэробной мощности работы.
Обезвоживание вызывает электролитный дисбаланс во всех
жидкостных системах организма. Происходит значительная потеря минералов.
Значительная потеря электролитов особенно сказывается на нарушении проведения
нервного импульса в клетку и ее ответной реакции. При этом повышается уровень
глюкозы в крови при неизмененном плазменном глицерине, концентрации свободных
жирных кислот. Избыточное содержание глюкозы в крови возможно за счет увеличения
скорости утилизации гликогена в печени (как опосредованная реакция на
обезвоживание) и истощения его запасов.
Именно поэтому необходимо использовать напитки во время
выполнения длительных физических нагрузок. В последнее время в спорте как
правило используются напитки, которые содержат комплексы легкоусвояемых
углеводов, органических кислот, витаминов, минералов, незаменимых аминокислот и
ненасыщенных жирных кислот. При составлении спортивных напитков
широко используются и полимеры глюкозы.
Большое значение имеет процентное содержание
глюкозо-электролитных растворов. 8-10% раствор практически сразу же всасывается,
что значительно повышает функциональные возможности организма. Температура
напитков, возмещающих потерю жидкости, должна быть 8-13 °С, так как охлаждение
полости рта способствует оптимизации терморегуляции и увеличению скорости
всасывания жидкости.
Количество жидкости, принимаемой для восполнения потерь,
лимитируется скоростью всасывания из ЖКТ – не более 800 мл/ч, хотя потеря может
составлять значительно большее количество.
Использование напитков на дистанции (где возможно) или на
тренировке во время выполнения длительных физических нагрузок абсолютно
необходимо. Вариант приема: 200—400 мл перед нагрузкой, далее – 100—250 мл
каждые 10-15 минут.
Проконтролировать потерю жидкости можно взвешиванием до и
после нагрузки: общая потеря веса минус 1 кг составляет величину дефицита
жидкости в организме.
Оксиданты
Одна из главных причин интенсификации реакций
свободно-радикального повреждения элементов клеток при гипоксии – это природа
первичных радикалов, образующихся в клетке, и особенность их взаимодействия с
элементами клеточных структур.
Клеточные органеллы, а также сама клетка имеют избыточный
отрицательный заряд. Первичные радикалы, появляющиеся в клетке в результате
окислительных реакций, являются супероксидными ион-радикалами и также
отрицательно заряжены. Будучи высоко подвижными, они устремляются из митохондрий
сначала в цитоплазму, а затем в межмембранное пространство. Движущая сила,
направляющая поток кислорода из клетки в межклеточное пространство,
характеризуется величиной мембранного потенциала. Ионы кислорода выводятся из
клетки по принципу электрофореза. При гипоксии по мере снижения величины
мембранного потенциала ион-радикалы задерживаются в клетке, что ведет к
ускорению процессов окислительной деструкции клеточных элементов и способствует
наступлению терминальной фазы гипоксии.
Первое сообщение о свободных радикалах (оксидантах),
обнаруженных в живых тканях, появилось в 1931 г. Впоследствии было зафиксировано
целое семейство свободных радикалов, появляющихся и играющих разнообразные роли
в биологических тканях.
Основные группы оксидантов: супероксидные радикалы,
перекись водорода, гидроксильные радикалы, жирные пероксирадикалы и атомарный
кислород. Выявленные продукты представляют пеструю группу разнообразных по
природе веществ, характеризующихся одним общим признаком – наличием на одном из
атомов неспаренного электрона. Как правило, такое состояние вещества неустойчиво,
и свободные радикалы стремятся превратиться в стабильные продукты путем
спаривания свободного электрона. Это достигается либо путем отрыва атома (чаще
всего атома водорода) от другого соединения и присоединения его к радикалу, либо
за счет реакции рекомбинации, связанной с соединением двух радикалов в одну
молекулу. Выбираемый способ самоуничтожения зависит от активности свободного
радикала, т е. от его способности участвовать в отщеплении атома (водорода) от
соседних молекул.
По этому признаку свободные радикалы условно делятся на
активные и стабильные.
Активные радикалы отличаются агрессивным поведением
по отношению к своим соседям. Время их жизни невелико, и они быстро исчезают,
взаимодействуя с одной из близлежащих молекул. Результатом такого взаимодействия
становится отрыв атома водорода и появление нового радикала. Такой процесс
называют реакцией передачи цепи. Именно в результате таких
взаимодействий в клетке развиваются деструктивные процессы, сопровождающиеся
повреждением биологических мембран, молекул ДНК и белков.
Стабильные радикалы, появляющиеся в биологических
объектах, правильнее было бы назвать условно-стабильными. Такие радикалы не
способны отрывать атомы водорода от большинства молекул, входящих в состав
клетки. Но они могут совершать подобную операцию с особыми молекулами, имеющими
слабо связанные атомы водорода. Последний класс химических соединений получил
название антиоксидантов, поскольку механизм их действия основан на торможении
свободнорадикальных процессов в тканях. Время жизни стабильных радикалов
достаточно продолжительно.
Принципиальное различие в химическом поведении обоих
классов радикалов определяет столь же принципиальное различие их влияния на
многие физиологические и биохимические процессы в клетке. Если активные
свободные радикалы способствуют росту энтропии (нестабильности) в биологических
тканях, что ведет к развитию патологических состояний, ускоренному старению
организма и его смерти, то стабильные радикалы тормозят развитие деструктивных
процессов, замедляют старение и гибель клеток.
Появление активных кислородсодержащих радикалов связано с
окислительными процессами. Поскольку интенсивность их протекания в биологических
тканях неоднородна, то и зоны локального появления свободных радикалов очень
гетерогенны. На уровне клетки до 60% всех выявленных радикалов образуются в
митохондриях. Это связано с тем, что данные органеллы – главные
энергопреобразующие системы клетки. Именно через них проходят основные потоки
метаболизируемого кислорода. До 20% генерируемых в клетке радикалов образуются в
микросомах, где осуществляется химическая переработка многих чужеродных для
организма продуктов, включая лекарственные препараты. Оставшиеся 20% радикалов
приходятся на остальные структуры клетки.
В спорте в результате запредельных нагрузок,
неблагоприятных факторов внешней среды и действия "внешних" оксидантов
происходит инициация свободнорадикальных процессов, их резкая активизация.
Свободные радикалы способствуют образованию токсических продуктов, нарушающих
функцию клеточных мембран и биоэнергетических механизмов.
Интенсивная физическая нагрузка приводит к сбоям природных
механизмов контроля, нарушениям в антиоксидантной системе. Количество свободных
радикалов резко возрастает, разрушая клеточные структуры и организм в целом.
Антиоксиданты
В настоящее время система антиоксидантной защиты клеток от
токсичных форм кислорода и продуктов неполного его восстановления изучена и
напоминает линию обороны, где каждый рубеж представлен определенным
антиоксидантом, при этом в работе отдельных антиоксидантов прослеживается не
закон случая, а согласованная работа всего ансамбля антиоксидантов. Несмотря на
многочисленные исследования в данной области, сейчас нет уверенности, что
современная наука достигла полной ясности в понимании этой сложной проблемы.
Однако основные принципы работы системы антиоксидантной защиты известны и все
шире применяются на практике.
Наличие в клетке двух несмешивающихся фаз – водной и
ли-пидной – определило принципиальное разделение антиоксидантов на водо-
и липорастворимые. Первые предназначены для защиты содержимого
цитоплазмы и внутриклеточных органелл, крови, лимфы и других биологических
жидкостей от реакций самопроизвольного окисления. Вторые выполняют функции
антиоксидантов в биологических мембранах и липидсодержащих частицах, например в
липопротеинах. Возможность одновременного присутствия в каждой из фаз нескольких
типов радикалов, различающихся по активности, предусматривает наличие группы
антиоксидантов, обеспечивающих эффективное связывание любого из появляющихся
радикалов в любой из имеющихся фаз.
В настоящее время выяснено, что роль антиоксидантов не
сводится только к взаимодействию с органическими радикалами и прерыванию ПОЛ. К
числу антиоксидантов теперь относят и вещества, препятствующие развитию
окислительных процессов.
Такие вещества (в отличие от антиоксидантов прямого
действия, непосредственно взаимодействующих со свободными радикалами) относятся
к превентивным антиоксидантам, препятствующим самому появлению свободных
радикалов и развитию цепных реакций. Основные направления их действия связаны со
структурированием мембран, что создает дополнительные трудности в развитии
процессов ПОЛ, либо с ограничением возможности распада перекисей по
свободнорадикальному механизму. В последнем случае превентивные антиоксиданты
либо переводят перекиси в неактивные продукты (спирты, альдегиды или кетоны),
либо связывают ионы металлов переменной валентности, что затрудняет распад
перекисей на свободные радикалы. Таким образом, число веществ, рассматриваемых в
настоящее время в качестве антиоксидантов, значительно расширилось, однако
основное внимание обычно уделяется антиоксидантам прямого действия, среди
которых выделяют низкомолекулярные антиоксиданты и ферменты антиоксидантной
защиты.
В системе антиоксидантной защиты биологических молекул в
водной фазе наиболее заметную роль играет глутатион. Последний относится
к низкомолекулярным антиоксидантам и состоит из трех аминокислот: у-глутаминовой
кислоты, цистеина и глицина.
В плазме крови основным тиолом, выполняющим функции
ан-тиоксиданта, является аминокислота цистеин. Хотя содержание последней
в плазме крови почти на порядок уступает концентрации глутатиона в цитоплазме,
ее более высокая реакционная способность как аминокислоты (по сравнению с
трипептидом) обеспечивает эффективную защиту биологических структур,
контактирующих с кровью, от повреждающего воздействия свободных радикалов. В
результате реакции со свободными радикалами цистеин превращается в цистин.
Другим эффективным антиоксидантом, присутствующим в
заметном количестве в плазме крови, является аскорбиновая кислота, или
витамин С.
Дефицит аскорбиновой кислоты в организме негативно
сказывается на процессах образования коллагена (от чего зависит прочность
костей, зубов, стенок кровеносных сосудов), процессах репарации тканей.
Аскорбиновая кислота – эффективная ловушка для большинства
активных кислородсодержащих радикалов. Она настолько эффективна, что способна
регенерировать а-токоферол (витамин Е) из токоферильного радикала, образующегося
на первой стадии окисления витамина Е. Таким образом, аскорбиновая кислота может
участвовать в антиоксидантной защите тканей от повреждающего действия радикалов
как непосредственно, выполняя роль ловушки таких радикалов, так и опосредованно
путем восстановления токоферильных радикалов до витамина Е. Данный пример
иллюстрирует тесное взаимодействие водо– и липорастворимых антиоксидантов.
При активации выброса катехоламинов в кровь последние
наряду со своей прямой гормональной функцией выполняют роль антиоксидантов.
Образующиеся в результате взаимодействия катехоламинов со свободными радикалами
продукты токсичны (особенно для клеток нервной системы). Отсюда становится
понятной физиологическая потребность человека в движении при эмоциональном
стрессе. Только в этом случае стимулируется кровообращение и обеспечивается
быстрое выведение нейротоксинов из тканей и их инактивация в печени. Люди,
которые не выполняют этого простого требования природы, впоследствии
расплачиваются своим здоровьем.
Отличительная особенность защиты внутриклеточных элементов
от повреждающего действия свободных радикалов по сравнению с плазмой крови
состоит в широком использовании ферментов, инактивирующих радикалы и перекиси.
Считается, что ферменты антиоксидантной защиты внутри клеток выполняют основную
нагрузку по нейтрализации этих продуктов и являются первой линией обороны от
радикалов.
В отличие от низкомолекулярных антиоксидантов ферментная
система антиоксидантной защиты оказалась не столь универсальной. Из всех
возможных кислородсодержащих радикалов последняя оказалась способной связывать
только наименее активные супероксидные ион-радикалы. Задача по уничтожению
наиболее активных и в биологическом отношении наиболее опасных радикалов
разрешима только при участии низкомолекулярных антиоксидантов.
Из липорастворимых ловцов свободных радикалов наибольшее
внимание в научной литературе уделяется а-токоферолу, или витамину Е. Его
антиоксидантные функции в первую очередь связаны со способностью отдавать свой
атом водорода активному радикалу, превращаясь при этом в малоактивный радикал –
токоферил. Витамин Е – еще одна ловушка для всех активных кислородсодержащих
радикалов. Особая структура молекулы обеспечивает витамину Е возможность
встраиваться в фосфолипидные мембраны и прерывать протекающие в них процессы
перекисного окисления липидов.
Обычно концентрация а-токоферола в тканях достигает 10-50
мкМ. При таких концентрациях витамин Е проявляет свойства антиоксиданта. Однако
при концентрациях выше физиологических он проявляет противоположные свойства, т
е. является проок-сидантом и способствует ускорению ПОЛ. Такой двойной эффект
связан с природой токоферильного радикала. При низких концентрациях витамина
образующиеся токоферильные радикалы успевают быстро восстановиться до исходного
а-токоферола за счет взаимодействия с аскорбиновой кислотой или другим сильным
восстановителем. Но при высоких концентрациях витамина Е образующиеся радикалы
не успевают восстанавливаться и образуют комплексы с продуктами перекисной
природы, ускоряя распад последних по свободнорадикальному механизму.
Витамин Е концентрируется в печени и оттуда с кровью
направляется на периферию. Поскольку витамин не растворим в воде, для его
доставки используются специальные транспортные белки. Содержание водорастворимой
формы витамина составляет около 1 мкМ. Обмен антиоксидантами между водной и
липидной фазами позволяет контролировать общий уровень процессов ПОЛ в обоих
субстанциях. Считается, что на долю витамина Е приходится ингибирование до
10-20% от всех реакций ПОЛ в клетке.
Важную роль в защите биомембран от окислительной
биодеградации играет другой жирорастворимый витамин – витамин А и его заменитель
из растительного сырья – (3-каротин. Оба продукта – очередная линия обороны для
защиты синглетного кислорода.
Убихинон выполняет функцию не только обязательного
участника в работе митохондриальной дыхательной цепи, но и функцию эффективного
антиоксиданта. Убихинон несколько уступает по активности а-токоферолу. По этой
причине при протекании окислительных процессов в мембранах вначале расходуется
а-токоферол и лишь после исчерпания его запасов начинает использоваться более
дефицитный убихинон.
Поддержание высокой активности ферментов дыхательной цепи –
основное условие эффективной защиты митохондриальной мембраны от
свободнорадикального повреждающего воздействия активных форм кислорода. При
снижении активности таких ферментов, например, в условиях гипоксии, создаются
благоприятные условия для повреждения митохондриальных мембран.
Прием антиоксидантов способствуют прекращению негативных
явлений окисления в организме и повышению работоспособности (табл. 23).
В практике спорта в качестве антиоксидантов и веществ,
повышенное содержание которых способствует более эффективному действию
антиоксидантов, применяются следующие препараты:
• витамины А, С, Е, В5 , (B-каротин)
• адаптогены;
• мед, пыльца;
• гинкго-билоба, плюща вьющегося листья;
• олифен, кофермент Q-10 (убихинон), селен, нейробутал,
три-овит, оксилик, энзимы.
Применение антиоксидантов
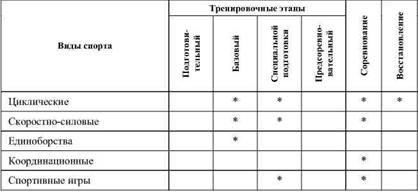
Витамин А (ретинол) . Жирорастворимый
витамин. Играет важную роль в окислительно-восстановительных процессах
(вследствие большого количества ненасыщенных связей). Участвует в синтезе
мукополисахаридов, белков, липидов. Ретинолу принадлежит важная роль в
поддержании нормального состояния кожи и эпителия слизистых оболочек,
обеспечении нормальной дифференциации эпителиальной ткани, в процессах
фоторецепции (способствует адаптации человека к темноте). Ретинол участвует в
минеральном обмене, процессах образования холестерина, усиливает выработку
липазы и трипсина, усиливает миелопоэз, процессы клеточного деления. Местное
действие обусловлено наличием на поверхности клеток эпителия специфических
ретинолсвязывающих рецепторов. Препарат омолаживает клеточные популяции и
уменьшает количество клеток, идущих по пути терминальной дифференцировки.
Показания. Профилактика перетренировки в видах
спорта на выносливость, скоростно-силовых видах. Гиповитаминоз и авитаминоз А.
Заболевания глаз. Заболевания и поражения кожи (отморожения, ожоги, раны,
гиперкератоз, псориаз, некоторые формы экземы, воспалительные и дегенеративные
патологические процессы). Комплексная терапия ОРЗ, хронических бронхолегочных
заболеваний, эрозивно-язвенных и воспалительных поражений ЖКТ.
Применение. Назначают внутрь, в/м, наружно.
Лечебные дозы при авитаминозах легкой и средней степени: взрослым – до 33 000 ME
в сутки; детям – 1000—5000 ME в сутки в зависимости от возраста.
Масляные растворы можно также применять наружно – при
ожогах, язвах, отморожениях, смазывая пораженные участки 5-6 раз в сутки,
прикрывая марлей; одновременно назначают ретинол внутрь или в/м.
Примечание. Гиперавитаминоз А: у взрослых –
сонливость, вялость, головная боль, гиперемия лица, тошнота, рвота, расстройства
походки, болезненность в костях нижних конечностей. У детей возможны повышение
температуры, сонливость, потливость, рвота, кожные высыпания.
Противопоказания. Желчнокаменная болезнь,
хронический панкреатит (возможно обострение заболевания); беременность (I
триместр).
Витамин Е (а-токоферол) . Оказывает
антиоксидантное действие. Участвует в биосинтезе гема и белков, пролиферации
клеток, тканевом дыхании, других важнейших процессах тканевого метаболизма,
предупреждает гемолиз эритроцитов, препятствует повышенной проницаемости и
ломкости капилляров.
Показания в спорте. Большой объем и интенсивность
физических нагрузок. Перетренированность. Неблагоприятные метеоусловия.
Заболевания связочного аппарата и мышц. Посттравматическая, постинфекционная
вторичная миопатия. Дегенеративные и пролиферативные изменения суставов и
связочного аппарата позвоночника и крупных суставов. Состояния после
перенесенных заболеваний, протекавших с лихорадочным синдромом. Вегетативные
нарушения. Астено-невротический синдром при переутомлении.
Применение. Обычно назначают по 100—300 мг в сутки.
Побочное действие: аллергические реакции; при
приеме больших доз – диарея, боли в эпигастрии.
Селен. Микроэлемент. Антиоксидант. Является
существенной частью ферментной системы глутатион пероксидазы, влияет на
активность фермента. Глутатион пероксидаза защищает внутриклеточные структуры от
повреждающего действия свободных кислородных радикалов, которые образуются как
при обмене веществ, так и под влиянием внешних факторов, в том числе
ионизирующего излучения. Недостаток селена в организме может привести к развитию
кардиомиопатии и других сердечно-сосудистых заболеваний. В настоящее время селен
рассматривают как перспективный антиканцерогенный фактор.
Показания. Восстанавливающее средство при
неблагоприятном воздействии физической перегрузки, неблагоприятных воздействиях
окружающей среды на спортсмена (при дефиците селена в организме).
Применение. Взрослым и детям старше 7 лет назначают
по 100 мкг в сутки.
Побочное действие. В редких случаях возможны
аллергические реакции. Противопоказан при повышенной чувствительности к
препаратам селена.
Не следует превышать рекомендуемые дозы препарата. При
появлении запаха чеснока в выдыхаемом воздухе (симптом передозировки селена)
препарат следует отменить.
Причинами нарушения микроциркуляции и изменений текучести
крови при занятиях в спорте могут быть: запредельная физическая нагрузка при
неблагоприятных внешних факторах, которая приводит к повреждению эндотелия
сосудов; травма.
Следствием может стать нарушение свертывающей системы крови
(развитие синдрома диссеминированного внутрисосудистого свертывания –
ДВС-синдрома; тканевая гипоксия; нарушение функций внутренних органов: сердца,
печени, почек и т. д.).
Выявление и контроль присходят путем исследования
коагулограммы, рН крови, гематокрита, вязкости крови. Исследуется осадок мочи на
наличие патологических продуктов обмена. Анализируется ЭКГ с целью обнаружения
метаболических сдвигов и очаговых поражений в миокарде.
Для коррекции применяются препараты, улучшающие
микроциркуляцию и реологические свойства крови, влияющие на свертываемость
крови.
Микроциркуляция
Кровь представляет собой особую систему в человеческом
организме, обеспечивая доставку кислорода, пластических, энергетических,
информационных веществ к каждой клетке. От реологических свойств крови
(текучесть), возможности ее прохождения по микрососудам, капиллярам зависит
жизнь клеток и всего организма в целом.
Система гемостаза, как и другие биологические системы
организма, обеспечивающие гомеостаз (постоянство внутренней среды организма),
обладает высокой пластичностью и надежностью, в силу чего она не только успешно
адаптируется ко многим физиологическим и патогенным влияниям, но и в широких
пределах коррегирует нарушения жизнедеятельности организма – поддерживает
целостность и замкнутость сосудистой системы, объем, жидкое состояние и
некоторые другие свойства циркулирующей крови.
В общепатологических закономерностях процессов повреждения
внутрисосудистое свертывание крови и агрегация тромбоцитов занимают значительное
место, являясь неспецифическим и/или специфическим компонентом и в развитии
патологии, и во влиянии на восстановление нарушенных функций.
ДВС-синдром
Крайним выражением нарушений микроциркуляции и реологии
крови во время напряженной физической работы при неблагоприятных условиях
(высокая температура воздуха, влажность, перепады атмосферного давления)
является ДВС-синдром.
В настоящее время все большее распространение получают
соревнования в видах спорта, требующих не просто выносливости, а
сверхвыносливости, – марафоны в различных видах спорта (триатлон, суточный бег,
экстремальные виды спорта и т д.), что требует от спортсменов идеального
здоровья. При этом лимитирующим звеном становится неспособность системы
микроциркуляции обеспечивать нормальный обмен в клетках и тканях.
В спорте могут возникнуть и другие провоцирующие состояния,
при которых происходит внутрисосудистое свертывание крови: шок травматический;
острая кровопотеря; тепловой удар; повреждение сосудистой стенки физической
нагрузкой в экстремальных условиях; гипоксия с дезорганизацией стенок
микрососудов; блокада микроциркуляции в жизненно важных органах – легких,
печени, почках, надпочечниках; прием контрацептивов, гемопре-паратов (эритропоэтин
– ЭПО), глюкокортикоидов; появление в плазме грубых продуктов распада и
поврежденных клеток крови.
При ДВС-синдроме наблюдаются фазовые изменения в
свертывающей системе крови:
I фаза – гиперкоагуляция (тромбообразование);
II фаза – гипокоагуляция (кровоточивость).
Резкая активация свертывающей системы крови, значительное
поступление в кровь тканевого тромбопластина или других активаторов
гемокоагуляции могут вызвать Д ВС-синдром, который, в свою очередь, может
привести к тромбогеморрагическому синдрому.
При ДВС-синдроме образуются тромбы по всему организму, в
первую очередь в системе микроциркуляции. Процесс может протекать хронически,
клинически стерто. В этих условиях кровотечения нередко становятся ведущим
проявлением нарушения гемостаза, а предшествующая и фоновая гиперкоагуляции
остаются замаскированными и плохо выявляемыми.
Анализ исследований, посвященных изучению данного вопроса,
позволяет заключить, что ДВС-синдром встречается значительно чаще, чем об этом
принято думать. Поэтому применение препаратов, нормализующих микроциркуляцию и
условия протекания крови по сосудам при длительных, экстремальных нагрузках,
является насущной проблемой.
В период интенсивных тренировочных нагрузок можно
рекомендовать прием препаратов, способствующих улучшению микроциркуляции и
реологических свойств крови.
Вессел дуэ ф (сулодексид). Естественная
смесь двух гликоза-миногликанов, состоящая из гепариноподобной фракции (80%) и
дерматан сульфата (20%). Эти отрицательно заряженные суль-фатированные
мукополисахариды обладают широким спектром биологической активности.
Комплексный механизм действия данного препарата обусловлен
его двухкомпонентным составом:
1) быстротекущая гепариноподобная фракция имеет сродство к
антитромбину III – физиологическому антикоагулянту, участвующему в торможении
процесса свертывания крови;
2) дерматиновая фракция имеет сродство к кофактору гепарина
II – второму ингибитору тромбина.
Фармакологические свойства. Вессел дуэ ф оказывает
антитромботическое, профибринолитическое, антикоагулянтное и вазопротективное
виды действия на уровне макро– и микрососудов.
Способствует уменьшению вязкости крови вследствие снижения
содержания фибриногена в плазме и антиагрегационного действия.
Обладает выраженным антитромботическим действием как в
артериальных, так и в венозных сосудах. В связи с низкой антикоагулянтной
активностью сулодексид препятствует образованию тромбов, не увеличивая риск
кровотечения.
Обладает существенной профибринолитической активностью,
которая обусловлена увеличением продукции простагландинов, усилением выделения
тканевого активатора плазминогена в просвет сосудов и уменьшением содержания в
крови ингибитора тканевого активатора плазминогена.
Подавляет пролиферацию гладкомышечных клеток сосудистой
стенки, способствует восстановлению структуры и функции клеток эндотелия сосудов,
нормализует реологические свойства крови.
Препятствует прогрессированию атеросклероза кровеносных
сосудов за счет уменьшения содержания липидов (главным образом триглицеридов) в
крови, подавлению пролиферации и миграции гладкомышечных клеток субэндотелия.
Способствует сохранению функциональных свойств и
морфологической целостности эндотелия капилляров и базальной мембраны почечных
клубочков.
Препарат повышает содержание и активность липолитическо-го
фермента – липопротеинлипазы в циркулирующей крови, в результате чего снижается
уровень холестерина, ЛПНП, триглицеридов при умеренном повышении уровня
холестерина ЛПВП.
90% сулодексида абсорбируется в эндотелии сосудов, что
превышает его концентрацию в тканях других органов в 20-30 раз. Всасывается в
тонком кишечнике.
Метаболизируется в печени и почках. Препарат претерпевает
экстрацеллюлярную диффузию в печени и почках через 4 ч после введения. Через 24
ч после в/в введения экскреция препарата с мочой составляет 50% соединения, а
через 48 ч – 67%.
Показания в спорте. С целью повышения
работоспособности при максимальной нагрузке, особенно в подготовке спортсменов в
условиях среднегорья (при повышении гематокрита, повышенном количестве
эритроцитов); для профилактики осложнений гемостаза микрососудистого русла при
повышенной вязкости крови. Лечение нарушений гемореологии и коррекции физической
работоспособности в спорте высших достижений, ангиопатий с повышенным риском
образования тромбов, нарушений мозгового кровообращения, флебопатий, тромбозов
глубоких вен, микроангио-патий, антифосфолипидном синдроме.
Побочные действия. Со стороны ЖКТ возможны тошнота,
рвота, боли в эпигастрии. Аллергические реакции: кожная сыпь различной
локализации. Местные реакции: боль, жжение, гематома в месте инъекции (0,5-1% от
общего числа пациентов).
В случае необходимости терапия препаратом контролируется
общими коагуляционными тестами.
Не рекомендуется одновременно использовать препараты,
влияющие на систему гемостаза в качестве антикоагулянтов (прямых и непрямых) и
антиагрегантов.
Гинкго-билоба (танакан). Средство
растительного происхождения. Влияет на обмен веществ в клетках, реологические
свойства крови и микроциркуляцию, а также на вазомоторные реакции крупных
кровеносных сосудов. Улучшает мозговое кровообращение и снабжение мозга
кислородом и глюкозой. Обладает сосудорасширяющим действием, препятствует
агрегации тромбоцитов. Нормализует метаболические процессы, оказывает
антиги-поксическое действие на ткани. Препятствует ПОЛ и образованию свободных
радикалов клеточных мембран. Оказывает выраженное противоотечное действие на
уровне головного мозга и в периферических тканях. При различных патологических
состояниях предотвращает усиление протеолитической активности сыворотки.
Применение. При нарушениях периферического
кровообращения и микроциркуляции при тяжелой физической нагрузке; астеническом
состоянии (в том числе обусловленном травматическими поражениями головного мозга
в травмоопасных видах спорта); черепно-мозговых травмах, психогенной и
невротической депрессии при перетренировке, для профилактики ДВС-синдрома при
марафонах. При дисциркуляторной энцефалопатии различного генеза, проявляющейся
расстройствами внимания и/или памяти, снижением интеллектуальных способностей,
чувством страха, нарушениями сна. При нейросенсорных нарушениях (головокружении,
звоне в ушах).
Побочное действие: расстройства пищеварения,
головные боли, аллергические реакции.
Трентал (пентоксифиллин, агапурин, вазонит).
Улучшает микроциркуляцию и реологические свойства крови, оказывает
сосудорасширяющее действие, блокирует фосфодиэстеразу и способствует накоплению
АМФ в клетках. Повышает эластичность эритроцитов,
уменьшает их адгезию, уменьшает агрегацию тромбоцитов и вязкость крови.
Блокирует аденозиновые рецепторы.
Применение: в напряженный период тренировок, при
"горной" подготовке, тренировке в условиях жаркого климата; нарушениях
периферического кровообращения (марафоны); в случае трофических нарушений в
тканях (в том числе при отморожениях).
Побочные действия: диспептические явления, тошнота,
рвота, сердцебиение, тахикардия, гиперемия кожных покровов, головокружение,
головная боль, нервозность, сонливость или бессонница, кожные аллергические
реакции, изредка повышенная ломкость ногтей, изменение массы тела, отеки,
кровотечения.
При назначении препарата следует контролировать уровень АД.
Совместимость раствора пентоксифиллина с инфузионным раствором следует проверять
в каждом конкретном случае до начала введения. Потенцирует действие
гипотензивных средств, инсулина, пероральных гипогликемизирующих препаратов.
Дозу пентоксифиллина в этих случаях следует несколько уменьшить. При назначении
одновременно с антикоагулянтами необходимо тщательно следить за показателями
свертывания крови.
Кавинтон (винпоцетин). Препарат, улучшающий
микроциркуляцию, переносимость гипоксии, улучшающий мозговое кровообращение и
мозговой метаболизм. Способствует транспортировке кислорода к тканям вследствие
уменьшения сродства к нему эритроцитов, усиливая поглощение и метаболизм
глюкозы; уменьшает повышенную вязкость крови. Метаболизм глюкозы переключается
на энергетически более выгодное аэробное направление. Стимулирует также и
анаэробный метаболизм глюкозы.
Показания: острая и хроническая недостаточность
мозгового кровообращения (транзиторная ишемия в видах спорта на выносливость);
посттравматическая и гипертензивная энцефалопатия (травоопасные виды спорта);
для уменьшения нарушений памяти; при головокружении, головной боли, двигательных
расстройствах.
Курантил (персантин, дипиридамол, тромбонил).
Снимает спазм гладкой мускулатуры. Сосудорасширяющее
средство.
Применяются также: боярышника плоды, вобэнзим, дезагреганты
(папаверин, эуфиллин) и т д.
Основными причинами снижения иммунной реактивности
организма спортсмена в основном являются:
– запредельная физическая нагрузка;
– неблагоприятные метеоклиматические условия;
– психоэмоциональная перегрузка – стресс.
Следствием снижения иммунной защиты становится
подверженность заражению любым инфекционным заболеванием в период максимальных
нагрузок или предсоревновательный период, или во время соревнований.
Для определения состояния иммунной системы проводятся
контрольные исследования.
Коррекция проводится с применением иммунокорректоров;
адаптогенов; витаминов; аминокислот (незаменимые).
Иммунитет
Иммунитет – способ защиты внутреннего постоянства организма
от генетически чужеродной информации (антигены, токсины).
Иммунологическая реактивность организма спортсмена зависит
от объема и интенсивности физических и психоэмоциональных нагрузок. Резервные
возможности иммунной системы, осуществляя эффективную защиту организма от
инфекций при незначительных физических нагрузках, при нарастании
мышечно-эмоционального стресса, характерного для нагрузок современного "большого
спорта", истощаются, и у спортсмена появляется состояние иммунодефицита.
Вторичным иммунодефицитом может обернуться и недостаток питания (или
несбалансированное питание) при определенных диетах. Кроме того, иммунитет
заинтересован в витаминах А, С, Е, микроэлементах, играющих важную роль в его
нормальном функционировании.
Коррекция иммунного статуса спортсмена
Напряжение иммунитета зависит от величины и
продолжительности нагрузки и проходит следующие фазы: мобилизация, компенсация,
декомпенсация, восстановление. Резервные возможности иммунной системы в первые
две фазы (мобилизации и компенсации) еще обеспечивают эффективную защиту
организма. Переход в третью фазу (декомпенсация) обусловлен нарастанием
мышечно-эмоционального стресса, характерного для нагрузок при современных
методиках подготовки спортсмена.
Режимы нагрузок, при которых наступает фаза истощения
резервных возможностей иммунной системы, индивидуальны для каждого спортсмена,
зависят от многих факторов, в том числе и его генотипа. Это обстоятельство
делает бесспорной необходимость контроля иммунного статуса при профессиональных
занятиях спортом.
Профилактические мероприятия, помогающие избежать срыва
иммунитета:
– санация очагов хронической инфекции, поскольку постоянная
интоксикация резко снижает резервные возможности организма;
– выявление и лечение дисбактериоза;
– защита от психоэмоционального стресса;
– постоянная поддержка баланса витаминов, микроэлементов,
белков, жиров, углеводов, аминокислот для полноценного обеспечения иммунной
системы энергетическими и пластическими субстратами;
– четкое ведение тренировочного процесса по физиологическим
возможностям конкретного спортсмена;
– специальная иммунокоррекция при длительных переездах
(перелетах), тренировке в горах и т. д.
Профилактические средства. Прием препаратов,
обладающих выраженным регулирующим действием на обменные процессы, в том числе
на иммунитет, помогает его восстановлению.
Это продукты пчеловодства: апилак, апилактоза, мед с
пергой, сотовый мед многолетней экспозиции; препараты из цветочной пыльцы:
гранулированная цветочная пыльца, политабс, цернилтон, тенториум плюс.
Неспецифические биогенные стимуляторы: адаптогены, масло облепихи, мумиё,
бета-каротин. Поливитаминные комплексы с обязательным содержанием витаминов
группы В, фолиевой и аскорбиновой кислоты.
Лекарственные средства, стимулирующие иммунитет
Интерфероны – альфаферон, веллферон,
интерферон, интрон-А, реальдерон, ребиф, роферон.
Индукторы синтеза интерферонов – амиксин,
полудан, ридостин, тилорон, циклоферон.
Интерлейкины – интерлейкин-2, пролейкин,
ронколейкин.
Иммуностимулирующие – синтетические:
декарис, дибазол, инозин пранобекс, левамизол, ликопид, метилурацил,
полиоксидоний, тимоген.
Препараты комбинированного состава –
вобэнзим, синупрет, тонзилгон.
Бактериальные – бронхомунал, имудон,
рибомунил.
Иммуностимуляторы животного происхождения –
тактивин, тималин, тимостимулин, имунофан.
Фитопрепараты – иммунал (эхинацея),
иммунорм, эстифан.
Коррекция иммунодефицитных состояний
Чаще всего
применяют: иммуномодулирующие препараты – тималин, тимоген, Т-активин;
препараты, стимулирующие выработку интерферона – циклоферон, ронколейкин; другие
препараты курсами
Циклоферон. Обладает противовоспалительным,
противовирусным, иммуностимулирующим действием. Нормализует выработку
интерферона, способствует коррекции иммунного статуса организма при
иммунодефицитах и аутоиммунных состояниях. Стимулирует продукцию лейкоцитами,
макрофагами, эпителиальными клетками, а также тканями селезенки, печени, легких,
мозга. Проникает в цитоплазму и ядерные структуры, активирует синтез "ранних"
интерферонов. Отличается низкой токсичностью и отсутствием мутагенных и
канцерогенных эффектов. При парентеральном введении быстро и полностью
всасывается. Незначительно связывается с белками. Легко проникает в органы,
ткани и биологические жидкости (в том числе ликвор). 99% введенного препарата
выводится почками в неизмененном виде в течение 24 ч. Не кумулируется даже при
длительном применении.
Применяется при иммунодефицитных состояниях различного
происхождения (в том числе обусловленных физическим перенапряжением), а также:
дегенеративно-дистрофических заболеваниях суставов (деформирующий остеоартроз и
др.); инфекциях бактериальных, герпетических; острых и хронических вирусных
гепатитах (А, В, С, D); ревматоидном артрите; язвенной болезни желудка и
двенадцатиперстной кишки; кожных заболеваниях (нейродерматит, экзема,
дерматозы).
Применение. Взрослым: раствор для инъекций, в/м,
в/в, разовая доза – 0,25-0,5 г; таблетки внутрь за 30 мин до еды, не
разжевывая, – 0,3-0,6 г 1 раз в сутки. Курс: 1, 2, 4, 6, 8, 11, 14, 17, 20, 23,
26, 29-й день. Профилактика – 1, 2, 4, 6, 8-й день.
Противопоказания: декомпенсированный цирроз печени,
детский возраст (до 4-х лет), беременность.
Побочных действий при применении циклоферона не
выявлено.
Совместим со всеми лекарственными средствами (в том числе
антибиотиками, витаминами, иными иммуномодуляторами).
Эхинацея (иммунал). Средство растительного
происхождения. Оказывает иммуномодулирующий, противовоспалительный эффекты.
Полисахариды, содержащиеся в эхинацее, повышают фагоцитарную активность
нейтрофилов и макрофагов, стимулируют продукцию интерлейкина-1. Комплекс
действующих веществ индуцирует трансформацию В-лимфоцитов в плазматические
клетки, улучшает функции Т-хелперов. Благодаря инулину, левулезе, бетаину
улучшаются обменные процессы, особенно в печени и почках.
Показания: вторичный иммунодефицит при значительной
физической нагрузке; психическое и физическое переутомление; им-мунодефицитные
состояния при хронических рецидивирующих воспалительных заболеваниях различной
локализации; состояние после антибиотикотерапии.
Препараты эхинацеи принимают внутрь. Дозировка и
длительность применения устанавливаются индивидуально, в зависимости от
используемой лекарственной формы. Чаще всего по 20 кап. 2-3 раза в день внутрь
после еды, 2 недели.
Побочное действие: возможны аллергические реакции;
при применении в высоких дозах возможны тошнота, рвота, нарушения стула,
бессонница, повышенная возбудимость нервной системы.
Противопоказания: повышенная чувствительность к
препаратам эхинацеи; аутоиммунные заболевания; с осторожностью применяют при
нарушении углеводного обмена.
Недостаточное функционирование эндокринной системы может
быть вызвано широким спектром причин – от генетических до инфекционных. Причиной
дисфункции может стать и введение гормональных препаратов. (Гормональные
препараты запрещены к употреблению в спортивной практике, расцениваются как
допинг.)
Вмешательства в эндокринный статус часто оборачиваются
нарушением всех видов обмена.
Выявление и контроль осуществляется определением
составляющих гормонального профиля.
Коррекция дисбаланса эндокринной системы проводится
специфическими методами, соответствующими выявленной причине, построением
специальной диеты.
Гормоны
Одной из регуляторных систем организма является система
гормональной регуляции. Отличительная ее особенность – использование химического
кода.
Эндокринные железы выделяют специальные химические
вещества, названные гормонами, которые содержат определенную информацию,
передаваемую другим клеткам (табл. 27). Гормоны с кровью и лимфой переносятся по
всему организму в поисках своих адресатов – клеток-мишеней. Клетки-мишени
характеризуются наличием особых структур (рецепторов), расположенных на наружной
поверхности мембран и способных из потока разнообразной информации выделить
необходимую, предназначенную для данного типа клеток. Такой механизм позволяет
строго избирательно воздействовать на определенные органы.
Все переносимые с биологическими жидкостями химические
сигналы условно разделяются на две большие группы: водо- и
жирорастворимые. Такое деление удобно не только по формальному признаку их
растворимости в той или другой среде, сколько различает их по механизму действия
на клетку-мишень.
Белки-рецепторы находятся либо внутри клеток, либо встроены
в клеточную мембрану. Рецепторы для всех водорастворимых переносчиков химических
сигналов локализованы на наружной поверхности клеточных мембран. Механизм, с
помощью которого дошедший до клетки химический сигнал вызывает внутри клетки
каскад биохимических изменений, в общих чертах стандартный, но может различаться
на заключительных стадиях.
Например, для адреналина и глюкагона рецептором является
мембраносвязанный, встроенный в клеточную мембрану фермент аденилатциклаза.
Присоединение гормона к этому ферменту приводит к повышению его каталитической
активности. Под действием активированной аденилатциклазы имеющийся внутри клеток
АТФ превращается в АМФ. Образовавшийся АМФ непосредственно участвует в регуляции
клеточного метаболизма.
Клетки органов-мишеней содержат ферменты, разрушающие
поступающие в них гормоны и цАМФ, что ограничивает действие гормонов во времени
и предупреждает их накопление.
Краткая характеристика отдельных гормонов
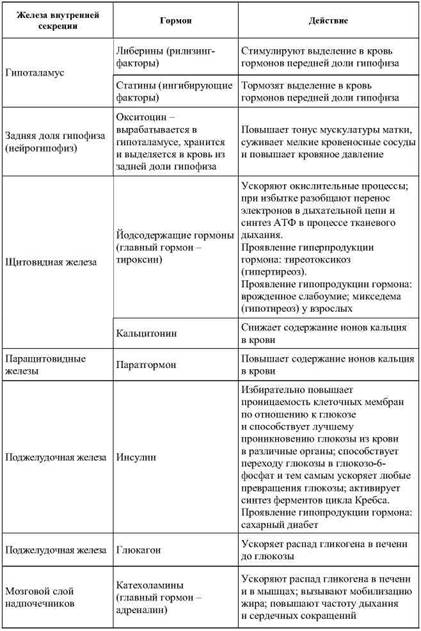
Окончание таблицы
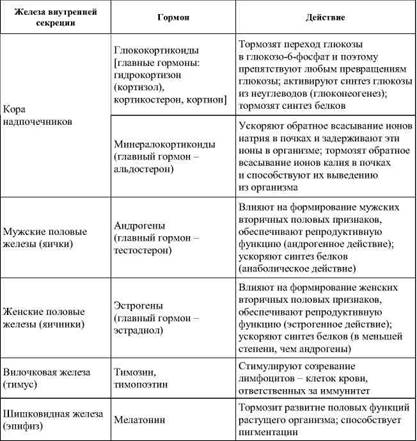
Чувствительность рецепторов и активность ферментов,
расщепляющих гормоны, может меняться при нарушениях обмена, изменениях
физико-химических параметров организма (температура, кислотность, осмотическое
давление), концентрации важнейших субстратов, при выполнении мышечной работы,
заболеваниях, введении лекарственных средств. Следствием этого является усиление
или ослабление влияния гормонов на соответствующие органы.
Механизмы действия гормонов разнообразны, среди них можно
выделить главные, присущие большинству гормонов:
1) гормоны влияют на скорость синтеза ферментов, ускоряя
или замедляя его: в органах-мишенях повышается или снижается концентрация
определенных ферментов, изменяя скорость ферментативных реакций;
2) гормоны влияют на активность ферментов в этих органах,
являясь:
– активаторами ферментов – скорость ферментативных реакций
повышается;
– ингибиторами ферментов – скорость ферментативных реакций
снижается;
3) гормоны влияют на проницаемость клеточных мембран в
отношении определенных химических соединений: в клетки поступает больше или
меньше субстратов для ферментативных реакций, что тоже обязательно сказывается
на скорости химических процессов.
Таким образом, основные действия гормонов направлены на
регуляцию скорости химических реакций в клетках и оказывают влияние на
физиологические функции.
По химическому строению гормоны делятся на группы.
Гормоны белковой природы (белки и полипептиды):
– гормоны гипоталамуса,
– гормоны гипофиза,
– кальцитонин щитовидной железы,
– гормон паращитовидных желез,
– гормоны поджелудочной железы.
Гормоны – производные аминокислоты тирозина:
– йодсодержащие гормоны щитовидной железы,
– гормоны мозгового слоя надпочечников.
Гормоны стероидного строения:
– гормоны коры надпочечников,
– гормоны половых желез.
Синтез и выделение гормонов в кровь находятся под контролем
нервной системы. В упрощенном виде взаимосвязь между эндокринной и нервной
системами можно представить следующим образом. При воздействии на организм
каких-либо внешних факторов или же при возникновении изменений в крови и в
различных органах соответствующая информация передается по чувствительным нервам
в гипоталамус (орган ЦНС). В ответ на полученную информацию вырабатываются
гормоны гипоталамуса, которые затем поступают в гипофиз и стимулируют или
тормозят в нем секрецию гормонов передней доли гипофиза. Гормоны выделяются из
гипофиза в кровь, переносятся в железы внутренней секреции и вызывают в них
синтез и секрецию соответствующих гормонов, которые далее воздействуют на
органы-мишени. Таким образом в организме осуществляется единая
нервно-гормональная, или нейрогуморальная, регуляция.
В частности, регуляция обмена углеводов может быть
представлена следующим образом (в основе лежит саморегуляция).
Концентрация глюкозы в периферической крови относится к
биологическим константам, т е. величинам, колебания которых не должны превышать
определенные гомеостатические нормы. У здорового человека содержание глюкозы в
состоянии относительного покоя находится в пределах 4,5-5,5 ммоль/л (80-120
мг%). Повышение уровня глюкозы выше 5,5 ммоль/л называется гипергликемией,
падение ниже 3,3 ммоль/л – гипогликемией. От избыточных потерь глюкозы организм
предохраняет функция почек: глюкоза, профильтровавшаяся в первичную мочу,
реабсорбируется из почечных канальцев в кровь, если только ее содержание в крови
не превышает 8,5 ммоль/л. Наличие глюкозы в моче называется глюкозурией.
Это означает, что более или менее значительное отклонение
концентрации глюкозы в крови от нормальных пределов возбуждает механизмы, под
влиянием которых происходит ее нормализация. Рассмотрим эти механизмы
саморегуляции на примере гипогликемии, гипергликемии.
Ведущая роль в контроле содержания глюкозы в крови
принадлежит гипоталамусу. Возбуждение гипоталамических центров приводит
к активированию физиологических механизмов, способствующих нормализации уровня
глюкозы в крови. К ним относятся возбуждение симпатического отдела нервной
системы и усиление секреции катехоламинов мозговым слоем надпочечников,
повышение продукции глюкагона а-клетками поджелудочной железы, а также
активирование гипоталамических либеринов, под влиянием которых вырабатываются
кортикотропин, глюкокортикоиды и соматотропин.
Гипогликемия – мощный стимулятор для усиления секреции
катехоламинов и глюкагона. Катехоламины (адреналин, норадреналин и
дофамин) попадают в периферическую кровь, где связываются с белком и циркулируют
в связанном виде. Свободные катехоламины быстро разрушаются под влиянием
ферментов. Катехоламины оказывают влияние на органы мишени через специфические
адренорецепторы.
Для регуляции уровня глюкозы в крови преимущественное
значение имеет адреналин. Он активирует распад гликогена в печени и мышцах.
Влияние на гликоген осуществляется через фосфорилазы. В печеночных клетках при
этом образуется избыток глюко-зофосфатов, а затем – свободной глюкозы, которая
поступает в кровь и противодействует гипогликемии. В мышцах под влиянием
адреналина происходит распад гликогена до глюкозы и молочной кислоты, которые
частично захватываются гепатоцитами, и восполняются запасы гликогена.
Определенное влияние, схожее с адреналином, оказывает
норад-реналин надпочечников и симпатических нервов. Однако интенсивность его
влияния на углеводный обмен значительно меньше.
Секрецию глюкагона стимулирует гипогликемия, а также
уменьшение содержания в крови жирных кислот и аминокислот. Существенное
тормозящее влияние на секрецию глюкагона оказывает соматостатин, вырабатываемый
в эндокринной части поджелудочной железы. Симпатический отдел нервной системы
активирует секрецию глюкагона. Это создает дополнительный стимул для выделения
его при гипогликемии. Ответная секреция глюкагона при значительном снижении
уровня глюкозы в крови происходит быстро и в значительных пределах (в 4-5 раз).
Глюкагон оказывает выраженное гипергликемическое действие,
которое делят на две фазы. Первая фаза – гликогенолиз, в основе которого
лежит активирование фосфорилазы; т е. аналогично действию адреналина. Однако, в
отличие от адреналина, глюкагон не действует на гликоген мышц, поэтому не
вызывает повышения содержания молочной кислоты в крови. Первая фаза
непродолжительна и зависит от количества гликогена, резервированного в печени.
Вторая фаза гипергликемии – четкое влияние глюкагона обусловлено
глюконеогенезом, т. е. новообразованием глюкозы из неуглеводных соединений.
Эта фаза характеризуется менее высоким, но более длительным повышением
концентрации глюкозы в крови.
Кортикотропин – глюкокортикоиды. Возбуждение
гипоталамических нейросекреторных клеток при гипогликемии охватывает центры
продукции кортиколиберина. По существу, значительное уменьшение уровня
всегда является острым стрессом. Увеличенное образование и выделение в
портальную систему гипофиза кортиколиберина неминуемо приводит к активированию
секреции кортикотропина из передней доли гипофиза, а под влиянием кортикотропина
стимулируется биосинтез глюкортикоидов в коре надпочечных желез. Основной
глюкокортикоид человека – кортизол, который активно усиливает распад
белка (кроме печени) и усиливает новообразование углеводов из неуглеводных
компонентов. Главным субстратом глюконеогенеза служат аминокислоты,
освобождающиеся из белков различных органов под влиянием тех же
глюкокортикоидов. В результате в печени увеличивается количество гликогена,
который поставляет глюкозу в кровь. Как видно, в отношении глюконеогенеза
глюкокортикоиды действуют синергично (однонаправленно) с глюкагоном.
Соматотропин. Гипогликемия – мощный стимулятор
секреции соматотропина. Его гипергликемическое действие объясняется уменьшением
потребления глюкозы периферическими тканями. Следует также помнить, что
анаболическое влияние соматотропина в белковом обмене требует участия инсулина,
поэтому его длительная повышенная секреция приводит к истощению инсулина.
Саморегулирование четко выражено и при гипергликемических
состояниях. Наиболее мощным фактором, противодействующим повышению уровня
глюкозы в крови, является инсулин. Глюкоза – специфический стимулятор
секреции этого гормона. Синтез инсулина происходит в (3-клетках поджелудочной
железы. Вначале на рибосомах образуется препроинсулин – одиночный пептид из
104—110 аминокислотных остатков. По мере дальнейшего прохождения по шероховатой
эндоплазматической сети часть молекулы отщепляется и остается проинсулин из
81-86 аминокислотных остатков. В результате этого расщепления образуются
инсулин, частично расщепленный проинсулин и С-пептид (часть молекулы
препроинсулина). Все эти гормональные формы депонируются в секреторных гранулах
(3-клеток путем полимеризации и комплек-сирования с цинком. В ответ на
гипергликемию происходит двухфазное выведение гормона: первая быстрая (в течение
1 мин после действия стимула) и вторая – спустя 20-30 мин. В первой фазе
секретируется инсулин, расположенный вблизи цитоплазматичес-кой мембраны, а во
второй фазе происходит транспорт гранул инсулина по системе микротрубочек и
микрофиламентов от аппарата Гольджи до цитоплазматической мембраны. Лишь затем
гормон выводится из (3-клетки. Опосредуют влияние глюкозного стимула АМФ,
метаболиты глюкозы и Са2 .
Поступивший в кровь инсулин циркулирует в двух формах –
свободной и связанной с белками. Свободный инсулин действует на мышцы, жировую
ткань, печень и мозг, а связанный – только на жировую ткань. Между связанным и
свободным инсулином имеется динамическое равновесие: при гипергликемии
увеличивается количество свободной фракции и уменьшается количество связанного
гормона, а при недостатке глюкозы преобладает связанный инсулин.
Усилению секреции инсулина способствуют также соматотропин,
кортикотропин, глюкокортикоиды, т е. гормоны с гипергликемическим эффектом.
Инсулин – единственный сахаропонижающий гормон, влияние его
многопланово. Он вызывает повышение проницаемости цитоплазматических мембран
клеток-мишеней к моносахаридам, особенно к глюкозе. В печени инсулин активирует
глюкокиназу, в связи с чем возрастает количество глюкозо-6-фосфата,
соответственно усиливается метаболизм углеводов. В печени наиболее интенсивно
происходит глюкогенез, поэтому увеличивается содержание гликогена. Инсулин
подавляет также распад печеночного гликогена (гликогенолиз), а также тормозит
глюконеогенез. Наконец, инсулин способствует превращению углеводов в жиры и в
конечном итоге определяет анаболические процессы в организме.
Все железы внутренней секреции функционируют согласованно и
оказывают друг на друга взаимное влияние. Введение в организм извне гормонов не
только сказывается на функции железы, вырабатывающей вводимый гормон, но и может
оказать негативное воздействие на состояние всей нервно-гормональной регуляции в
целом.
Неквалифицированное вмешательство в регуляцию этой сложной
системы оказывает негативное влияние на функции всего организма. Поэтому
использование гормональных препаратов в качестве допингов опасно для здоровья
спортсменов.
Только специалисты могут грамотно провести коррекцию
гормонального статуса: эндокринолог, андролог, гинеколог-эндокринолог (см.
"Актуальные проблемы женского спорта").
При подозрении на сбои в работе какой-либо железы
внутренней секреции необходимо детально исследовать ее функции. Контроль за
уровнем глюкозы (а значит, косвенно, и за работой инсу-лярного аппарата) до
нагрузки и во время нагрузки стал рядовым фактом. Уровень развития современного
спорта настоятельно требует введения, также, в повседневную практику
исследований уровня гормонов щитовидной железы, половых гормонов.
Кроме того, долгие годы существовало убеждение, что
выделение кодируемой информации является спецификой тканей эндокринной системы.
В настоящее время в этой области науки достигнут значительный прогресс,
свидетельствующий о том, что практически все ткани участвуют во взаимном обмене
информацией между собою, а число химических сигналов, выделяемых тканями и
кодирующих передаваемую информацию, намного превосходит число известных
гормонов.
Всего 4 страницы < 1 2 3 4 >
Опубликовано 12.07.2011










